题目内容
5.某小组欲探究SO2和Cl2能否发生反应,设计如图所示的实验装置进行实验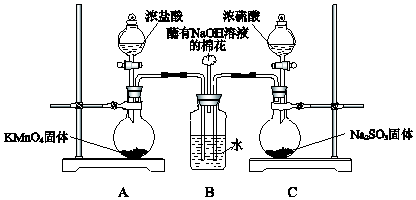
(1)装置A中的反应为2KMnO4+16HCl(浓)═2KCl+2MnCl2+5Cl2↑+8H2O,反应中氧化剂和还原剂的物质的量之比是1:5,生成71g Cl2时反应转移的电子是2 mol,装置C中生成SO2,反应的化学方程式是Na2SO3+H2SO4═Na2SO4+SO2↑+H2O
(2)装置B中蘸有NaOH溶液的棉花的作用是尾气处理,防止污染空气
(3)SO2与Cl2同时通入水中反应的化学方程式是SO2+Cl2+2H2O═2HCl+H2SO4.
分析 根据装置图分析可知:装置A是制备氯气的发生装置,装置C是制备二氧化硫的发生装置,氯气和二氧化硫通入装置B中的水,是否发生反应,设计实验教学分析验证,实质是二氧化硫和氯气在水中反应生成硫酸和氯化氢,注意氯气中的杂质气体分析和除杂.
(1)所含元素化合价降低的反应物为氧化剂;根据化学方程式中电子守恒计算生成71g Cl2转移的电子物质的量;装置C中浓硫酸与亚硫酸钠反应生成硫酸钠、二氧化硫与水;
(2)氯气有毒污染空气,不能排放需要用氢氧化钠吸收剩余氯气;
(3)二氧化硫和氯气同时通入水中发生氧化还原反应生成了盐酸和硫酸,由此书写化学反应方程式.
解答 解:(1)元素化合价升高的失电子做还原剂,元素化合价降低的做氧化剂,装置A中的反应为2KMnO4+16HCl(浓)═2KCl+2MnCl2+5Cl2↑+8H2O,反应中的氧化剂是KMnO4,反应中氧化剂和还原剂的物质的量之比是1:5,生成氯气5mol×71g/mol=355g,电子转移10mol,则生成71g Cl2转移的电子是2mol,装置C中浓硫酸与亚硫酸钠反应生成硫酸钠、二氧化硫与水,反应方程式为:H2SO4+Na2SO3=Na2SO4+SO2↑+H2O,
故答案为:1:5;2;Na2SO3+H2SO4═Na2SO4+SO2↑+H2O;
(2)氯气有毒污染空气,不能排放需要用氢氧化钠吸收剩余氯气,装置B中蘸有NaOH溶液的棉花的作用是吸收氯气尾气处理,防止污染空气,
故答案为:尾气处理,防止污染空气;
(3)二氧化硫和氯气同时通入水中发生氧化还原反应生成了盐酸和硫酸,化学方程式为:SO2+Cl2+2H2O═2HCl+H2SO4,故答案为:SO2+Cl2+2H2O═2HCl+H2SO4.
点评 本题考查了化学实验探究,物质性质、反应过程分析、离子检验和实验设计是解题关键,题目难度中等.

 三新快车金牌周周练系列答案
三新快车金牌周周练系列答案| A. | 溶液很快褪色,出现沉淀 | B. | 溶液不褪色,不出现沉淀 | ||
| C. | 溶液不褪色,出现沉淀 | D. | 溶液很快褪色,不出现沉淀 |
| A. | 镀锡铁表面划损时,仍然能阻止铁被腐蚀 | |
| B. | 锌和稀硫酸反应时,加人铜粉可使反应加快 | |
| C. | 将镁、铝用导线连接后放人NaOH溶液中,镁作负极 | |
| D. | 原电池负极上发生的反应是还原反应 |
| A. | x<y+z | B. | 平衡向正反应方向移动 | ||
| C. | A的转化率变大 | D. | C的体积分数变大 |
C(s)+H2O(g)=CO(g)+H2(g);△H=+131kJ•mol-1
2CO(g)+O2(g)=2CO2(g);△H=-564kJ•mol-1
2H2(g)+O2(g)=2H2O(g);△H=-482kJ•mol-1.
由以上反应推断往炽热的炉膛内通入水蒸气时( )
| A. | 不能节约燃料,但能使炉膛火更旺 | |
| B. | 虽不能使炉膛火更旺,但可节约燃料 | |
| C. | 既可使炉膛火更旺,又能节约燃料 | |
| D. | 既不能使炉膛火更旺,又不能节约燃料 |
| A. | 向盐酸酸化的Ba(NO3)2溶液中通入SO2,有白色沉淀生成,则BaSO3难溶于酸 | |
| B. | 液溴应保存在磨口玻璃塞的棕色细口试剂瓶中,并加少量水进行水封 | |
| C. | 用酒精萃取碘水中的碘,水从分液漏斗下口放出,碘的酒精溶液从分液漏斗上口倒出 | |
| D. | 蒸馏操作时,应使温度计水银球插入蒸馏烧瓶内的液面以下 |
| A. | 稀盐酸可除去烧瓶内残留的MnO2 | |
| B. | 稀硝酸可除去试管内壁的银镜 | |
| C. | Al2O3和MgO均可与NaOH溶液反应 | |
| D. | SO2和SO3混合气体通入Ba(NO3)2溶液可得到BaSO3和BaSO4 |
| A. | 该化合物的化学式为A2B | |
| B. | 该化合物的化学式为AB | |
| C. | 这种化合物中存在A2+和B3+两种微粒 | |
| D. | 这种化合物是离子化合物 |