题目内容
15.甲烷的一种氟化物的化学式是CH3F,下列说法正确的是( )| A. | 甲烷与氟气发生取代反应可以制得CH3F | |
| B. | CH3F分子中含有离子键 | |
| C. | CH3F分子中含有共价键和离子键 | |
| D. | CH3F的摩尔质量是34 |
分析 CH3F是共价化合物,只含共价键,是由甲烷和氟气发生取代反应而制取的,摩尔质量为34g/mol,据此分析.
解答 解:A、CH3F是由甲烷和氟气在光照条件下发生取代反应而制取的,故A正确;
B、CH3F是共价化合物,只含共价键,故B错误;
C、CH3F是共价化合物,不含离子键只含共价键,故C错误;
D、摩尔质量的单位为g/mol,故CH3F的摩尔质量为34g/mol,故D错误.
故选A.
点评 本题考查了CH3F的制取和化学键类型,难度不大,应注意的是摩尔质量的单位为g/mol.

练习册系列答案
相关题目
5.如表所示的五种元素中,W、X、Y、Z为短周期元素,这四种元素的原子最外层电子数之和为22.下列说法正确的是( )
| X | Y | ||
| W | Z | ||
| T |
| A. | 原子半径的大小顺序为:rZ>rW>rY>rX | |
| B. | 离子Y2-和X3-的核外电子数和电子层数都不相同 | |
| C. | 物质WY2、WZ4均有熔点高、硬度大的特性 | |
| D. | T元素的单质具有半导体的特性,T与Z元素可形成化合物TZ4 |
6.下列说法正确的是( )
| A. | 非自发反应在任何条件下都不能发生 | |
| B. | 冰融化为水的过程中△H<0,△S>0 | |
| C. | 2H2(g)+02(g)=2H2O(l)△H=-572kJ•mol-1此反应在低温时可以自发进行 | |
| D. | 知道了某过程有自发性之后,可预测过程发生完成的快慢 |
3.设NA为阿伏伽德罗常数的值.下列说法正确的是( )
| A. | 80mL10mol/L的浓盐酸与足量的MnO2加热反应,产生Cl2分子数约为0.2NA | |
| B. | 一定条件下,将1molN2和3molH2混合,充分反应后转移电子数为6NA | |
| C. | 钠在空气中燃烧可生成多种氧化物.23g钠充分燃烧时转移电子数为1NA | |
| D. | 常温常压下,等质量的CO和N2中含有原子数目均为2NA |
10.物质的转化在给定条件下能实现的是( )
| A. | NaCl(aq)$\stackrel{CO_{2}}{→}$NaHCO3(s)$\stackrel{△}{→}$Na2CO3(s) | B. | CuCl2$\stackrel{NaOH(aq)}{→}$Cu(OH)2$→_{△}^{乙醛}$Cu | ||
| C. | Al$\stackrel{NaOH(aq)}{→}$NaAlO2(aq)$\stackrel{△}{→}$NaAlO2(s) | D. | Al2O3(s)$\stackrel{HCl(aq)}{→}$AlCl3(aq)$\stackrel{通电}{→}$Al(s) |
10.下列说法错误的是( )
| A. | ns电子的能量可能低于(n-1)p电子的能量 | |
| B. | 6C的电子排布式1s22s22px2反了洪特规则 | |
| C. | 电子排布式(21Sc)1s22s22p63s23p63d3违反了能量最低原理 | |
| D. | 电子排布式(22Ti)1s22s22p63s23p10违反了泡利原理 |
7.关于下列各图的叙述正确的是( )

| A. | 甲中△H1=-(△H2+△H3) | |
| B. | 乙表示恒温恒容条件下发生的可逆反应2NO2(g)═N2O4(g)中,各物质的浓度与其消耗速率之间的关系,其中交点A对应的状态为化学平衡状态 | |
| C. | 丙表示A、B两物质的溶解度随温度变化情况,将tl℃时A、B的饱和溶液分别升温至t2℃时,溶质的质量分数B>A | |
| D. | 丁表示常温下,稀释HA、HB两种酸的稀溶液时,溶液pH随加水量的变化,则NaA溶液的pH大于等物质的量浓度的NaB溶液的pH |
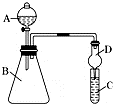 某同学欲利用图装置验证同主族元素性质递变规律.
某同学欲利用图装置验证同主族元素性质递变规律.