题目内容
能正确表示下列化学反应的离子方程式是( )
| A、过量的NaHSO4与Ba(OH)2溶液反应:Ba2++2OH-+2H++SO42-=BaSO4↓+2H2O |
| B、硫酸镁溶液跟氢氧化钡溶液反应:SO42-+Ba2+=BaSO4↓ |
| C、NH4HCO3溶液与过量NaOH溶液反应:NH4++OH-=NH3↑+H2O |
| D、向碳酸氢钠溶液中滴加少量稀硝酸:CO32-+2H +=CO2↑ +H2O |
考点:离子方程式的书写
专题:
分析:A.硫酸氢钠过量,氢氧化钡完全反应,离子方程式按照氢氧化钡的化学式组成书写;
B.硫酸镁与氢氧化钡溶液反应生成氢氧化镁和硫酸钡沉淀,漏掉了生成氢氧化镁沉淀的反应;
C.氢氧化钠过量,铵根离子、碳酸氢根离子都与氢氧根离子反应;
D.碳酸氢钠电离出钠离子和碳酸氢根离子,碳酸氢根离子在离子方程式中不能拆开.
B.硫酸镁与氢氧化钡溶液反应生成氢氧化镁和硫酸钡沉淀,漏掉了生成氢氧化镁沉淀的反应;
C.氢氧化钠过量,铵根离子、碳酸氢根离子都与氢氧根离子反应;
D.碳酸氢钠电离出钠离子和碳酸氢根离子,碳酸氢根离子在离子方程式中不能拆开.
解答:
解:A.过量的NaHSO4与Ba(OH)2溶液反应生成硫酸钡和水,反应的离子方程式为:Ba2++2OH-+2H++SO42-=BaSO4↓+2H2O,故A正确;
B.硫酸镁溶液跟氢氧化钡溶液反应生成硫酸钡和氢氧化镁沉淀,正确的离子方程式为:SO42-+Ba2++Mg2++2OH-=Mg(OH)2↓+BaSO4↓,故B错误;
C.NH4HCO3溶液与过量NaOH溶液反应生成一水合氨和碳酸根离子,正确的离子方程式为:HCO3-+NH4++2OH-=NH3?H2O+H2O+CO32-,故C错误;
D.向碳酸氢钠溶液中滴加少量稀硝酸,碳酸氢根离子不能拆开,正确的离子方程式为:HCO3-+2H+=CO2↑+H2O,故D错误;
故选A.
B.硫酸镁溶液跟氢氧化钡溶液反应生成硫酸钡和氢氧化镁沉淀,正确的离子方程式为:SO42-+Ba2++Mg2++2OH-=Mg(OH)2↓+BaSO4↓,故B错误;
C.NH4HCO3溶液与过量NaOH溶液反应生成一水合氨和碳酸根离子,正确的离子方程式为:HCO3-+NH4++2OH-=NH3?H2O+H2O+CO32-,故C错误;
D.向碳酸氢钠溶液中滴加少量稀硝酸,碳酸氢根离子不能拆开,正确的离子方程式为:HCO3-+2H+=CO2↑+H2O,故D错误;
故选A.
点评:本题考查了离子方程式的判断,为高考中的高频题,属于中等难度的试题,注意掌握离子方程式的书写原则,明确离子方程式正误判断常用方法:检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合守恒关系(如:质量守恒和电荷守恒等)、检查是否符合原化学方程式等.

练习册系列答案
 赢在课堂名师课时计划系列答案
赢在课堂名师课时计划系列答案 天天向上课时同步训练系列答案
天天向上课时同步训练系列答案
相关题目
下列物质属于含有共价键的离子化合物的是( )
| A、石墨 |
| B、NaOH |
| C、KF |
| D、CH4 |
下列电子式书写正确的是( )
A、溴化铵: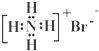 |
B、硫化氢: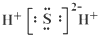 |
C、氮气: |
D、羟基: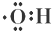 |
除去下列溶液中的杂质(括号内是杂质)所用试剂不正确的是( )
| A、KOH溶液[K2CO3]:用Ca(OH)2溶液 |
| B、NaOH溶液[Ba(OH)2]:用Na2SO4溶液 |
| C、NaCl溶液[Na2SO4]:用Ba(NO3)2溶液 |
| D、HNO3溶液[HCl]:用AgNO3溶液 |
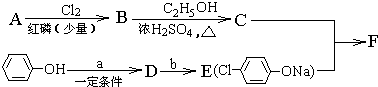
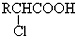 ,
,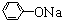 +RCl→
+RCl→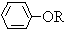 +NaCl
+NaCl