题目内容
H2O2在工业、农业、医药上都有广泛的用途.
(1)许多物质都可以做H2O2分解的催化剂.一种观点认为:在反应过程中催化剂先被H2O2氧化(或还原),后又被H2O2还原(或氧化).下列物质都可做H2O2分解的催化剂,在反应过程中先被氧化,后被还原的是 .
a、I- b、Fe3+ c、Cu2+ d、Fe2+
(2)用碱性氢氧燃料电池合成H2O2,具有效率高,无污染等特点.电池总反应为:H2+O2+OH-═H2O+HO2-.写出正极反应式: .
(3)H2O2是一种环境友好的强氧化剂.电镀废水(主要含Cu2+、Ni2+,还含少量Fe3+、Fe2+、Cr3+ 等)制备硫酸镍的一种流程如下:

①第(ⅰ)步,加入H2O2反应的离子方程式 .
②为测定NiSO4?nH2O的组成,进行如下实验:称取 2.627g样品,配制成250.00mL溶液.准确量取配制的溶液25.00mL,用0.04000mol?L-1的EDTA(Na2H2Y)标准溶液滴定Ni2+(离子方程式为Ni2++H2Y2-═NiY2-+2H+),消耗EDTA标准溶液25.00mL.则硫酸镍晶体的化学式为 .
(1)许多物质都可以做H2O2分解的催化剂.一种观点认为:在反应过程中催化剂先被H2O2氧化(或还原),后又被H2O2还原(或氧化).下列物质都可做H2O2分解的催化剂,在反应过程中先被氧化,后被还原的是
a、I- b、Fe3+ c、Cu2+ d、Fe2+
(2)用碱性氢氧燃料电池合成H2O2,具有效率高,无污染等特点.电池总反应为:H2+O2+OH-═H2O+HO2-.写出正极反应式:
(3)H2O2是一种环境友好的强氧化剂.电镀废水(主要含Cu2+、Ni2+,还含少量Fe3+、Fe2+、Cr3+ 等)制备硫酸镍的一种流程如下:

①第(ⅰ)步,加入H2O2反应的离子方程式
②为测定NiSO4?nH2O的组成,进行如下实验:称取 2.627g样品,配制成250.00mL溶液.准确量取配制的溶液25.00mL,用0.04000mol?L-1的EDTA(Na2H2Y)标准溶液滴定Ni2+(离子方程式为Ni2++H2Y2-═NiY2-+2H+),消耗EDTA标准溶液25.00mL.则硫酸镍晶体的化学式为
考点:化学电源新型电池,氧化还原反应,过氧化氢
专题:氧化还原反应专题,氧族元素
分析:(1)根据在反应过程中先被氧化,后被还原的即化合价先升高,后降低,结合元素的化合价来解答;
(2)碱性氢氧燃料电池工作时,电解质溶液是KOH溶液(碱性电解质),正极是O2得到电子,发生还原反应,正极的电极反应式为:O2+H2O+2e-=HO2-+OH-;
(3)①根据双氧水有强氧化性,能氧化还原性的物质,如Fe2+;
②根据关系式:NiSO4?nH2O~EDTA进行计算.
(2)碱性氢氧燃料电池工作时,电解质溶液是KOH溶液(碱性电解质),正极是O2得到电子,发生还原反应,正极的电极反应式为:O2+H2O+2e-=HO2-+OH-;
(3)①根据双氧水有强氧化性,能氧化还原性的物质,如Fe2+;
②根据关系式:NiSO4?nH2O~EDTA进行计算.
解答:
解:(1)a、I-的化合价可先升高到0价,再降低到-1价,符合题意;
b、Fe3+的化合价只能先降低,然后再升高,不符合题意;
c、Cu2+的化合价只能先降低,然后再升高,不符合题意,
d、Fe2+的化合价可先升高到+3价,再降低到+2价,符合题意,
故选:ad;
(2)碱性氢氧燃料电池工作时,正极是O2得到电子,发生还原反应,电极反应式为O2+H2O+2e-=HO2-+OH-,
故答案为:O2+H2O+2e-=HO2-+OH-;
(3)①双氧水有强氧化性,能氧化Fe2+,离子方程式为:2Fe2++H2O2+2H+=2Fe3++2H2O,
故答案为:2Fe2++H2O2+2H+=2Fe3++2H2O;
②NiSO4?nH2O~EDTA
0.001mol 0.04000mol?L-1×0.025L.
则250.00mL溶液中含有NiSO4?nH2O 0.01mol,即
=0.01mol,解n=6,所以硫酸镍晶体的化学式为NiSO4?6H2O,
故答案为:NiSO4?6H2O.
b、Fe3+的化合价只能先降低,然后再升高,不符合题意;
c、Cu2+的化合价只能先降低,然后再升高,不符合题意,
d、Fe2+的化合价可先升高到+3价,再降低到+2价,符合题意,
故选:ad;
(2)碱性氢氧燃料电池工作时,正极是O2得到电子,发生还原反应,电极反应式为O2+H2O+2e-=HO2-+OH-,
故答案为:O2+H2O+2e-=HO2-+OH-;
(3)①双氧水有强氧化性,能氧化Fe2+,离子方程式为:2Fe2++H2O2+2H+=2Fe3++2H2O,
故答案为:2Fe2++H2O2+2H+=2Fe3++2H2O;
②NiSO4?nH2O~EDTA
0.001mol 0.04000mol?L-1×0.025L.
则250.00mL溶液中含有NiSO4?nH2O 0.01mol,即
| 2.627g |
| (96+58.7+18n)g/mol |
故答案为:NiSO4?6H2O.
点评:本题是一道综合知识题目,涉及实验操作,电离方程式式、平衡常数、氧化还原反应,原电池、化学计算等,考查学生分析和解决问题的能力,难度较大.

练习册系列答案
 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案
相关题目
实验室有一瓶久置的K2SO3粉末,为确定其是否变质进行的下述实验结论正确的是( )
| A、进行元素分析,测得粉末中K和S两种元素的质量比为39:16,则该粉末没有变质 |
| B、将粉末溶于水,加入氯化钡,有白色沉淀生成,则该粉末变质了 |
| C、将粉末加入盐酸中,产生气泡,则该粉末没有变质 |
| D、将粉末溶于水,滴加过量的盐酸,有气泡产生,再加入氯化钡溶液,有白色沉淀生成,则该粉末部分变质 |
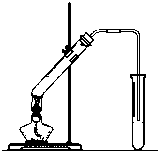 “酒是陈的香”,就是因为酒在储存过程中生成了有香味的乙酸乙酯,在实验室我们也可以用如图所示的装置制取乙酸乙酯.回答下列问题:
“酒是陈的香”,就是因为酒在储存过程中生成了有香味的乙酸乙酯,在实验室我们也可以用如图所示的装置制取乙酸乙酯.回答下列问题: