��Ŀ����
��ѧ�������о����ô�����������β���е�NO��COת���CO2��N2����ѧ����ʽ���£�2NO(g)+2CO (g)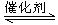 2CO2(g)+N2(g) ��H.
2CO2(g)+N2(g) ��H.
Ϊ�˲ⶨ��ij�ִ��������µķ�Ӧ�ٶȣ�ij�¶��£����ݻ�����������ڽ��д˷�Ӧ���������崫������ò�ͬʱ���NO��COŨ�������

��ش���������(���������¶ȱ仯�Դ�����Ч�ʵ�Ӱ��)��
(1)�ڸ÷�Ӧ��ƽ�ⳣ���ı���ʽK��________________��
(2)�÷�Ӧ�ڴ��¶����ܹ��Է����У�˵����H___________0(��д����������������������)��
��ֻ����Ӧ������Ϊ���ȣ�ƽ��ʱNO��Ũ�Ƚ�___________(���������С���������䡱)
(3)ǰ2s�ڵ�ƽ����Ӧ����v(N2)__________________.
(4)�о���������ʹ�õ���������ʱ����������ȱ���������ѧ��Ӧ���ʡ�Ϊ�˷ֱ���֤�¶ȡ������ȱ�����Ի�ѧ��Ӧ���ʵ�Ӱ����ɣ�ijͬѧ���������ʵ�飬����ʵ�������Ѿ���������ʵ����Ʊ��С�

�������ϱ��ո�������ʣ���ʵ���������ݡ�
�����ڸ���������ͼ�У��ο�ʵ��Iʵ�������»��������NOŨ����ʱ��仯����������ͼ������II��III������ͼ���������������ߵ�ʵ���š�

(ԭ��)��������ʵ����ʵ�����ܵõ���Ӧ���۵���
ѡ�� | ʵ����������� | ���� |
A | �����·ֱ����������Ũ�ȵĴ���Ͱ�ˮpH �����ֶ��ߵ�pH ֮��Ϊ14 | �����£�����Ͱ�ˮ�ĵ���ƽ�ⳣ����� |
B | ���ʢ��2mL5% H2O2 ��Һ����֧�Թ��зֱ����0.2mol/LFeCl3����0.3mol/L CuCl2 ��ҺlmL ��ǰ���������ݵ����ʸ��� | ��Ч����Fe3+��Cu2+ |
C | ��һ��Ũ�ȵĴ�����Һ�м���þ�����������ݵ��ʻ��ȼӿ��ټ��� | ��Ӧ�տ�ʼʱ���������ƽ�����ƣ�c(H+)���� |
D | ������(H3BO3 )��Һ�еμ�����Na2CO3��Һ���۲쵽�������� | H3BO3������ǿ��H2CO3 |


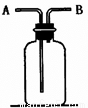
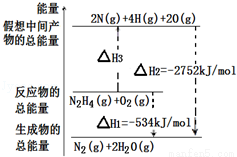
 H2(g)��2CO(g)����ƽ�����С���������ʹ��ϵ��ɫ����
H2(g)��2CO(g)����ƽ�����С���������ʹ��ϵ��ɫ���� 3��ƫ������(C2H8N2)���ӵ�����ԼΪ60g
3��ƫ������(C2H8N2)���ӵ�����ԼΪ60g