题目内容
0.1mol某烃在氧气中完全燃烧,将生成物全部通入浓硫酸中,浓硫酸增重9g,继续通入足量的澄清石灰水中,得到沉淀50g.
求:(1)该有机化合物的分子式
(2)若分子中只有两个甲基且属于不饱和烃,写出其结构简式.
求:(1)该有机化合物的分子式
(2)若分子中只有两个甲基且属于不饱和烃,写出其结构简式.
考点:有关有机物分子式确定的计算
专题:烃及其衍生物的燃烧规律
分析:(1)浓硫酸增重的为水的质量,50g沉淀为碳酸钙,可以先计算出水、二氧化碳的物质的量,然后根据质量守恒计算出该有机物的分子式;
(2)该烃的分子式为C5H10,若为不饱和烃,则其分子中含有1个碳碳双键,再根据其分子中含有两个甲基写出满足条件的结构简式.
(2)该烃的分子式为C5H10,若为不饱和烃,则其分子中含有1个碳碳双键,再根据其分子中含有两个甲基写出满足条件的结构简式.
解答:
解:(1)浓硫酸增重的为水的质量,0.1mol该烃完全燃烧生成水的质量为9g,其物质的量为:n(H2O)=
=0.5mol,n(H)=2n(H2O)=01mol,
50g沉淀为碳酸钙,碳酸钙的物质的量为:n(CaCO3)=
=0.5mol,n(CO2)=n(CaCO3)=0.5mol,
则该烃分子中含有C、H原子的数目分别为:
=5、
=10,
该烃的分子式为:C5H10,
答:该有机化合物的分子式C5H10;
(2)C5H10为不饱和烃,则分子中只能含有1个碳碳双键,即该烃为戊烯,只有两个甲基的戊烯的同分异构体有: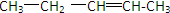 、
、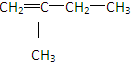 、
、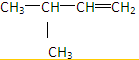 ,
,
答:该有机物的结构简式为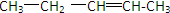 、
、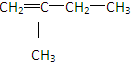 、
、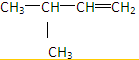 .
.
| 9g |
| 18g/mol |
50g沉淀为碳酸钙,碳酸钙的物质的量为:n(CaCO3)=
| 50g |
| 100g/mol |
则该烃分子中含有C、H原子的数目分别为:
| 0.5mol |
| 0.1mol |
| 1mol |
| 0.1mol |
该烃的分子式为:C5H10,
答:该有机化合物的分子式C5H10;
(2)C5H10为不饱和烃,则分子中只能含有1个碳碳双键,即该烃为戊烯,只有两个甲基的戊烯的同分异构体有:
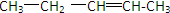 、
、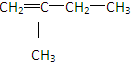 、
、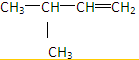 ,
,答:该有机物的结构简式为
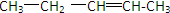 、
、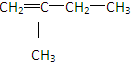 、
、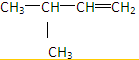 .
.
点评:本题考查了有机物分子式、结构简式的方法,题目难度中等,注意掌握确定有机物分子式、结构简式的常用方法,试题有利于提高学生的分析、理解能力及化学计算能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
如图操作正确的是( )
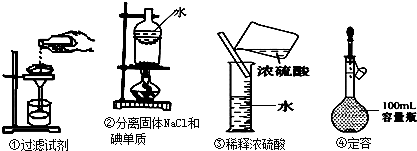

| A、② | B、②④ | C、①③ | D、全部不对 |
下列反应中Fe3+离子表现氧化性的是( )
| A、FeCl3溶液能使KI淀粉试纸变蓝 |
| B、FeCl3溶液滴入沸水中产生红褐色的胶体 |
| C、FeCl3溶液中加入AgNO3溶液产生白色沉淀 |
| D、FeCl3溶液中加入NaOH溶液产生红褐色沉淀 |
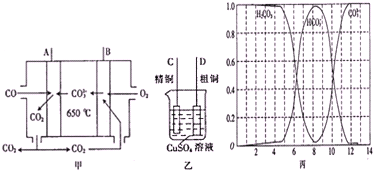
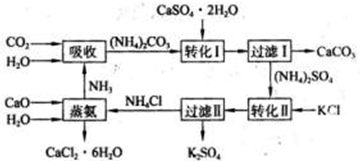
 空气质量与我们的健康息息相关,目前我国通过监测6项污染物的百分比浓度来计算空气质量指数(AQI),SO2、NO2和CO是其中3项中的污染物.
空气质量与我们的健康息息相关,目前我国通过监测6项污染物的百分比浓度来计算空气质量指数(AQI),SO2、NO2和CO是其中3项中的污染物.