题目内容
利用下列反应:Cu+2Ag+=Cu2++2Ag制一个化学电池(给出若干导线和一个小灯泡,电极材料和电解液自选),画出实验装置图,注明电解质溶液名称和正负极材料,标出电子流动方向和电流方向,写出电极反应式.(此题可以不做,做了且正确的额外加分)
【答案】分析:根据反应方程式中反应前后的金属单质确定电极材料,根据反应物中的化合物确定电解质.
解答:解:Cu+2Ag+=Cu2++2Ag,根据反应前后的金属单质确定电极材料,所以该原电池的电极材料是铜和银,铜比银易失去电子,所以铜作负极,银作正极;反应物中的化合物为含银离子的可溶性化合物,常见的有硝酸银,所以电解质溶液为硝酸银溶液;外电路中电子的流向为Cu→Ag,电流的流向为Ag→Cu.
故答案为: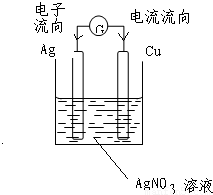
点评:原电池的设计:
1、基本方法
以氧化还原反应为基础,确定原电池的正负极、电解质溶液及电极反应,可参考锌-铜-稀硫酸原电池模型处理问题.其方法是还原剂作负极,不如负极活泼的金属或非金属导体作正极,氧化剂的溶液作电解质溶液.
2、电解质溶液的选择
电解质溶液一般要能与负极发生反应,或者是电解质溶液中溶解的其它物质与负极发生反应.
3、电极材料的选择
电极材料必须导电,负极必须能够与电解质溶液反应,容易失去电子;正极和负极之间只有产生电势差,电子才能定向运动,所以正极和负极不用同一种材料.
解答:解:Cu+2Ag+=Cu2++2Ag,根据反应前后的金属单质确定电极材料,所以该原电池的电极材料是铜和银,铜比银易失去电子,所以铜作负极,银作正极;反应物中的化合物为含银离子的可溶性化合物,常见的有硝酸银,所以电解质溶液为硝酸银溶液;外电路中电子的流向为Cu→Ag,电流的流向为Ag→Cu.
故答案为:

点评:原电池的设计:
1、基本方法
以氧化还原反应为基础,确定原电池的正负极、电解质溶液及电极反应,可参考锌-铜-稀硫酸原电池模型处理问题.其方法是还原剂作负极,不如负极活泼的金属或非金属导体作正极,氧化剂的溶液作电解质溶液.
2、电解质溶液的选择
电解质溶液一般要能与负极发生反应,或者是电解质溶液中溶解的其它物质与负极发生反应.
3、电极材料的选择
电极材料必须导电,负极必须能够与电解质溶液反应,容易失去电子;正极和负极之间只有产生电势差,电子才能定向运动,所以正极和负极不用同一种材料.

练习册系列答案
相关题目


