题目内容
20.某溶液中可能存在Br-、CO32-、SO32-、Al3+、I-、Mg2+、Na+等7种离子中的某几种.现取该溶液进行实验,得到如下现象:①向溶液中滴加足量氯水后,溶液变橙黄色,且有无色气泡冒出 ②向所得橙色溶液中加入足量BaCl2溶液,无沉淀生成 ③向所得溶液中继续滴加淀粉溶液,溶液不变蓝色.据此可以推断:该溶液中肯定不存在的离子组是( )| A. | Al3+ Mg2+ I- SO32- | B. | Mg2+ Na+ CO32- I- | ||
| C. | Al3+Na+ SO32- I- | D. | Na+ CO32- Br-I- |
分析 ①向溶液中滴加足量氯水后,溶液变橙黄色,说明溶液中有Br-;且有无色气泡冒出,说明溶液中有CO32-; 溶液中有CO32-,则无Al3+、Mg2+,根据溶液呈电中性,可知一定有Na+;②向所得橙色溶液中加入足量BaCl2溶液,无沉淀生成,说明溶液中无SO32-; ③向所得溶液中继续滴加淀粉溶液,溶液不变蓝色,说明无I-,据此进行解答.
解答 解:①向溶液中滴加足量氯水后,溶液变橙黄色,且有无色气泡冒出,则溶液中含有Br-、CO32-,由于CO32-与Al3+、Mg2+会发生反应而不能共存,所以一定不存在Al3+、Mg2+;
②因为若原溶液中含有SO32-,加入氯水时会氧化为SO42-,再加入足量BaCl2溶液,就会有沉淀生成,因此不存在SO32-;
③由于氯水会把I-氧化为I2继续滴加淀粉溶液,溶液就会变蓝色,因此该实验证明不存在I-.由于溶液呈电中性,所以还还有阳离子Na+;
根据上述实验证明在溶液中一定存在的离子为:Br-、CO32-、Na+,一定不存在Al3+ Mg2+ I- SO32-,
故选A.
点评 本题考查了常见离子的检验方法及离子共存的知识,题目难度中等,明确常见离子的性质及检验方法为解答关键,注意熟练掌握离子反应发生条件,试题培养了学生的分析能力及逻辑推理能力.

练习册系列答案
 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案
相关题目
10.在两个密闭容器中,分别充有质量相同的甲、乙两种气体,若两容器的温度和压强均相同,且甲的密度大于乙的密度,则下列说法正确的是( )
| A. | 甲的分子数比乙的分子数多 | |
| B. | 甲的摩尔体积比乙的摩尔体积小 | |
| C. | 甲的相对分子质量比乙的相对分子质量小 | |
| D. | 甲的物质的量比乙的物质的量少 |
11.下列各组的离子,能在溶液中大量共存的是( )
| A. | H+ PO3- K+ CO32- | B. | Ca2+ OH- Na+ CO32- | ||
| C. | K+NO3-NH4+Cl- | D. | Cu2+ F- Zn2+ OH- |
15.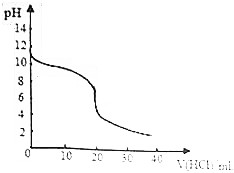 常温下,向20.00mL0.1000mol/L的氨水中逐滴加入0.1000mol/L的盐酸,pH随盐酸体积的变化如图所示.下列说法正确的是( )
常温下,向20.00mL0.1000mol/L的氨水中逐滴加入0.1000mol/L的盐酸,pH随盐酸体积的变化如图所示.下列说法正确的是( )
 常温下,向20.00mL0.1000mol/L的氨水中逐滴加入0.1000mol/L的盐酸,pH随盐酸体积的变化如图所示.下列说法正确的是( )
常温下,向20.00mL0.1000mol/L的氨水中逐滴加入0.1000mol/L的盐酸,pH随盐酸体积的变化如图所示.下列说法正确的是( )| A. | 滴加盐酸10mL 时,c(Cl-)>c(NH4+)>c(NH3•H2O)>c(OH-)>c(H+) | |
| B. | 滴加盐酸20m时,c(H+)=c(OH-)+c(NH3•H2O) | |
| C. | 滴加盐酸10 mL时溶液的导电能力与滴加盐酸20mL时溶液的导电能力相同 | |
| D. | pH<7时,消耗盐酸的体积一定大于20.00mL |
5.下列有关实验的说法正确的是( )
| A. | 为测定熔融氢氧化钠的导电性,可在氧化铝坩埚中熔化氢氧化钠固体后进行测量 | |
| B. | Fe(OH)3胶体可以将Fe Cl3滴入NaOH溶液中进行制备 | |
| C. | 除去铁粉中混有的少量铝粉,可加入过量的氢氧化钠溶液,完全反应后过滤 | |
| D. | 某溶液中加入盐酸能产生使澄清石灰水变浑浊的气体,则该溶液中一定含有CO32- |
9.有五瓶失去标签的溶液,它们分别为:①Ba(NO3)2;②KCl;③NaOH;④CuSO4;⑤Na2SO4;如果不用其它试剂(包括试纸),用最简便的方法将它们一一区别开来,则在下列鉴别顺序中最合理的是( )
| A. | ④③①⑤② | B. | ④⑤①③② | C. | ①⑤③④② | D. | ③④①⑤② |
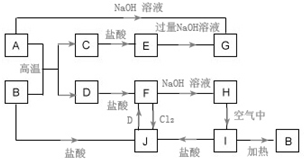
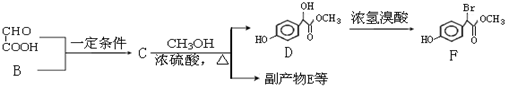
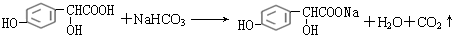 .
. .
.