题目内容
下表是不同温度下水的离子积常数:
试回答以下问题:
(1)若25<T1<T2,则a (填“>”、“<”或“=”)1×10-14,作出此判断的理由是 .
(2)25℃时,某Na2SO4溶液中c(SO42-)=5×10-4 mol/L,取该溶液1mL加水稀释至10mL,则稀释后溶液中c(Na+):c(OH-)= .
(3)T2℃下,将PH=11的苛性钠溶液V1与PH=1的稀硫酸V2L混合(设混合后溶液的体积为原两溶液体积之和),所得混合溶液的PH=2,则V1:V2= ,此溶液中各种离子的浓度由大到小的排列顺序是 .
| 温度/℃ | 25 | t1 | t2 |
| 水的离子积常数 | 1×10-14 | a | 1×10-12 |
(1)若25<T1<T2,则a
(2)25℃时,某Na2SO4溶液中c(SO42-)=5×10-4 mol/L,取该溶液1mL加水稀释至10mL,则稀释后溶液中c(Na+):c(OH-)=
(3)T2℃下,将PH=11的苛性钠溶液V1与PH=1的稀硫酸V2L混合(设混合后溶液的体积为原两溶液体积之和),所得混合溶液的PH=2,则V1:V2=
考点:离子积常数,pH的简单计算,盐类水解的应用
专题:
分析:(1)根据水的电离过程为吸热反应判断;
(2)硫酸钠溶液是显中性的;
(3)混合液的pH=2,酸过量,根据c(H+)=
计算,根据反应后溶液的组成分析各种离子的浓度大小.
(2)硫酸钠溶液是显中性的;
(3)混合液的pH=2,酸过量,根据c(H+)=
| n(H+)-n(OH-) |
| V总 |
解答:
解:(1)水是弱电解质,存在电离平衡,电离过程为吸热反应,所以温度升高,水的电离程度增大,离子积增大,
故答案为:>;升高温度,水的电离程度增大,离子积增大;
(2)25℃时,某Na2SO4溶液中c(SO42-)=5×10-4 mol/L,则溶液中钠离子浓度是1×10-3 mol/L.如果稀释10倍,则钠离子浓度是1×10-4 mol/L.但硫酸钠溶液是显中性的,所以c(Na+):c(OH-)=10-4:10-7=1000:1,
故答案为:1000:1;
(3)混合液的pH=2,酸过量,c(H+)=c(H+)=
=
=0.01,
解之得:
=9:11,
c(Na+)=0.1×9/(9+11)=0.045mol/L
c(SO42-)=0.05×11/20=0.0275mol/L
c(H+)=0.01mol/L
硫酸过量溶液显酸性,c 则(H+)>c (OH-),
故溶液中各种离子的浓度由大到小的排列顺序是:c (Na+)>c (SO42-)>c (H+)>c (OH-),
故答案为:9:11;c(Na+)>c(SO42-)>c(H+)>c(OH-).
故答案为:>;升高温度,水的电离程度增大,离子积增大;
(2)25℃时,某Na2SO4溶液中c(SO42-)=5×10-4 mol/L,则溶液中钠离子浓度是1×10-3 mol/L.如果稀释10倍,则钠离子浓度是1×10-4 mol/L.但硫酸钠溶液是显中性的,所以c(Na+):c(OH-)=10-4:10-7=1000:1,
故答案为:1000:1;
(3)混合液的pH=2,酸过量,c(H+)=c(H+)=
| n(H+)-n(OH-) |
| V总 |
| 0.1mol/L×V2L-0.1mol/L×V1L |
| (V1+V2)L |
解之得:
| V1 |
| V2 |
c(Na+)=0.1×9/(9+11)=0.045mol/L
c(SO42-)=0.05×11/20=0.0275mol/L
c(H+)=0.01mol/L
硫酸过量溶液显酸性,c 则(H+)>c (OH-),
故溶液中各种离子的浓度由大到小的排列顺序是:c (Na+)>c (SO42-)>c (H+)>c (OH-),
故答案为:9:11;c(Na+)>c(SO42-)>c(H+)>c(OH-).
点评:本题考查了水的电离、溶液中离子浓度大小比较以及pH计算,题目难度中等,该题是高考中的常见题型,属于中等难度的试题;该题的关键是明确溶液中几个重要守恒关系,即电荷守恒、物料守恒和质子守恒.

练习册系列答案
相关题目
下列说法中正确的是( )
| A、常温下pH=7的溶液中:Fe3+、Mg2+、SO42-、Cl-能大量共存 |
| B、已知电离平衡常数:H2CO3>HClO>HCO3-,向NaClO溶液中通入少量二氧化碳:ClO-+CO2+H2O=HClO+HCO3- |
| C、一定温度下,1L0.5mol?L-1NH4Cl溶液中与2L0.25mol?L-1NH4Cl溶液含NH4+物质的量相同 |
| D、常温下水电离出c(H+)×c(OH-)=10-20的溶液中:Na+、ClO-、SO42-、NH4+可能大量共存 |
经测定某溶液中只含NH4+、C1-、H+、OH-四种离子,下列说法错误的是( )
| A、溶液中四种粒子之间可能满足:c(C1-)>c(H+)>c(NH4+)>c(OH-) |
| B、若溶液中粒子间满足:c(NH4+)>c(C1-)>c(OH-)>c(H+)则溶液中溶质一定为:NH4Cl和NH3?H2O |
| C、若溶液中粒子间满足:c(C1-)>c(NH4+)>c(H+)>c(OH-)溶液中溶质一定只有NH4Cl |
| D、若溶液中c(NH4+)=c(Cl-),则该溶液一定显中性 |
下列与化学反应能量变化相关的叙述正确的是( )
| A、生成物总能量一定低于反应物总能量 |
| B、应用盖斯定律,可计算某些难以直接测量的反应焓变 |
| C、人类利用的能量都是通过化学反应获得的 |
| D、在化学反应中只有燃烧反应才能放出热量 |
下列有关化学用语表示正确的是( )
A、CH4分子的球棍模型: | ||
B、Cl-离子的结构示意图: | ||
C、氟化钠的电子式: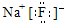 | ||
D、中子数为146、质子数为92 的铀原子
|