��Ŀ����
16����N2�� H2��һ��������ϣ�����ͬ״�������ܶ���H2�� 3.6����ȡ0.5mol�û������ͨ���ܱ������ڣ�ʹ֮������Ӧ����һ�������´ﵽƽ�⣮��֪��Ӧ�ﵽƽ���������ѹǿ����ͬ�����·�Ӧǰѹǿ��0.76����������1����Ӧǰ���������N2�� H2�������=1��4��
��2���ﵽƽ��ʱ��������еİ������ʵ���=0.06mol��
��3��ƽ��ʱN2��ת����=60%��
���� ��1��N2�� H2��һ��������ϣ�����ͬ״�������ܶ���H2��3.6������ƽ����Է�������Ϊ3.6��2=7.2���赪��Ϊxmol������Ϊymol����$\frac{28x+2y}{x+y}$=7.2���ݴ˽��м��㣻
��2���ɣ�1����֪��0.5mol�û�����壬���ʵ����ֱ�Ϊ0.1mol��0.4mol����
3H2+N2?2NH3��
��ʼ 0.4 0.1 0
ת�� 3n n 2n
ƽ��0.4-3n 0.1-n 2n
�ﵽƽ���������ѹǿ����ͬ�����·�Ӧǰѹǿ��0.76������$\frac{0.5-2n}{0.5}$=0.76����ð������ʵ�����
��3�����ݣ�2�����㵪����ת���ʣ�
��� �⣺��1��N2�� H2��һ��������ϣ�����ͬ״�������ܶ���H2��3.6������ƽ����Է�������Ϊ3.6��2=7.2��
�赪��Ϊxmol������Ϊymol����$\frac{28x+2y}{x+y}$=7.2�������ɵ�x��y=1��4��
��ͬ���������ʵ���֮�ȵ������֮�ȣ��������Ϊ1��4��
�ʴ�Ϊ��1��4��
��2���ɣ�1����֪��0.5mol�û�����壬���ʵ����ֱ�Ϊ0.1mol��0.4mol����
3H2+N2?2NH3��
��ʼ 0.4 0.1 0
ת�� 3n n 2n
ƽ��0.4-3n 0.1-n 2n
�ﵽƽ���������ѹǿ����ͬ�����·�Ӧǰѹǿ��0.76������$\frac{0.5-2n}{0.5}$=0.76��
��ã�n=0.06mol��
�ʴ�Ϊ��0.06mol��
��3��ƽ��ʱN2��ת����Ϊ��$\frac{0.06mol}{0.1mol}$��100%=60%��
�ʴ�Ϊ��60%��
���� ���⿼�黯ѧƽ��ļ��㣬Ϊ��Ƶ���㣬��Ŀ�Ѷ��еȣ���ȷ��ѧƽ�����η�����ĸ�ʽ��ƽ����Է���������ת���ʵļ��㼴�ɽ�𣬲��ؿ���ѧ���ķ�����������ѧ����������

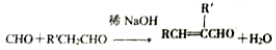 ��R��R���ʾ�������⣩
��R��R���ʾ�������⣩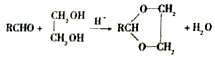
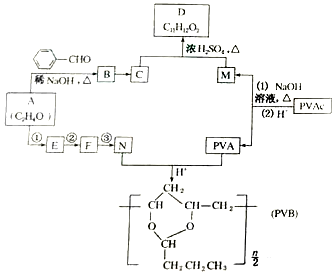
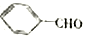 �ϳ�B�Ļ�ѧ����ʽ��
�ϳ�B�Ļ�ѧ����ʽ��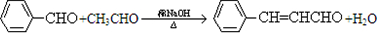 ��
��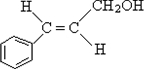 ��
��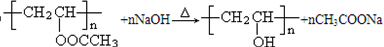 ��
��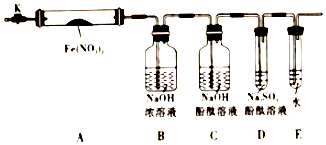 ���������μ����ֽ��Ҳ���ϸ��ӣ�ijѧϰС����Fe��NO3��2Ϊ�о�����ͨ��ʵ��̽�����ȷֽ�IJ���������ϣ��������������ȷֽ�Ĺ��ɣ��������4�ֲ��룺
���������μ����ֽ��Ҳ���ϸ��ӣ�ijѧϰС����Fe��NO3��2Ϊ�о�����ͨ��ʵ��̽�����ȷֽ�IJ���������ϣ��������������ȷֽ�Ĺ��ɣ��������4�ֲ��룺 ��1mol I2��g�� ��2mol H2����2L�ܱ������У���һ���¶��·�����Ӧ��I2��g��+H2��g��?2HI��g����H��0������ƽ�⣮HI���������w��HI����ʱ��仯��ͼ���ߣ�����ʾ��
��1mol I2��g�� ��2mol H2����2L�ܱ������У���һ���¶��·�����Ӧ��I2��g��+H2��g��?2HI��g����H��0������ƽ�⣮HI���������w��HI����ʱ��仯��ͼ���ߣ�����ʾ��

 +H2O
+H2O
 ��E�к��������ŵ����ƣ��Ȼ���
��E�к��������ŵ����ƣ��Ȼ��� +
+ $��_{��}^{ŨH_{2}SO_{4}}$
$��_{��}^{ŨH_{2}SO_{4}}$ +H2O��
+H2O��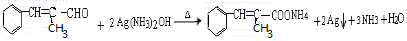 ��
�� ��
��