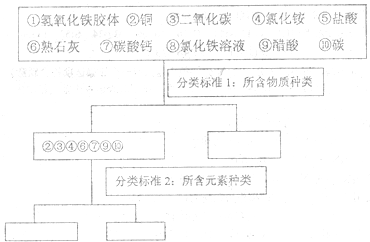
题目内容
10.将190gNa2CO3与NaHCO3的混合物加热使其充分反应,经浓硫酸干燥后,测得气体为11.2L(标况),问:(1)混合物中Na2CO3的质量是多少克?
(2)充分反应后,剩余固体的质量为多少克?
分析 (1)固体加热时发生2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O,由充分反应生成的气体可计算混合物中NaHCO3质量,再计算碳酸钠的质量;
(2)反应后剩余固体为碳酸钠,根据碳酸氢钠的质量计算出其分解生成的碳酸钠,从而可计算出反应后剩余固体的质量.
解答 解:(1)设混合物中碳酸氢钠的质量为m,则:
2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O
168g 106g 22.4L
m 11.2L
所以m=$\frac{11.2L×168g}{22.4L}$×168g=84g,
则混合物中碳酸钠的质量为:190g-84g=106g,
答:混合物中Na2CO3的质量是106g;
(2)充分加热后剩余固体为碳酸钠,84g碳酸氢钠分解生成碳酸钠的质量为:$\frac{84×106}{168}$g=53g,
则剩余固体的质量为:106g+53g=159g,
答:充分反应后,剩余固体的质量为159g.
点评 本题考查了混合物反应的计算,题目难度中等,明确发生反应的实质为解答关键,注意掌握物质的量与摩尔质量、气体摩尔体积之间的关系,试题培养了学生的分析能力及化学计算能力.

练习册系列答案
相关题目
20.观察下列几个装置示意图,有关叙述不正确的是( )


| A. | 装置①中阴极上析出红色固体 | |
| B. | 装置②的待镀铁制品应与电源负极相连 | |
| C. | 装置③中a为负极,发生的电极反应式为H2+2OH-+2e-═2H2O | |
| D. | 装置④中在阴极可以得到氢气和氢氧化钠,离子交换膜可选用阳离子交换膜 |
18.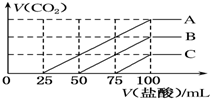 浓度相同的NaOH溶液各100mL倒入A、B、C三个烧杯中,分别向三份溶液中通入不等量的CO2,充分反应后,再向三份所得溶液中逐滴加入0.2mol•L-1的盐酸,产生CO2的体积与所加盐酸体积之间关系如图所示.下列判断正确的是( )
浓度相同的NaOH溶液各100mL倒入A、B、C三个烧杯中,分别向三份溶液中通入不等量的CO2,充分反应后,再向三份所得溶液中逐滴加入0.2mol•L-1的盐酸,产生CO2的体积与所加盐酸体积之间关系如图所示.下列判断正确的是( )
 浓度相同的NaOH溶液各100mL倒入A、B、C三个烧杯中,分别向三份溶液中通入不等量的CO2,充分反应后,再向三份所得溶液中逐滴加入0.2mol•L-1的盐酸,产生CO2的体积与所加盐酸体积之间关系如图所示.下列判断正确的是( )
浓度相同的NaOH溶液各100mL倒入A、B、C三个烧杯中,分别向三份溶液中通入不等量的CO2,充分反应后,再向三份所得溶液中逐滴加入0.2mol•L-1的盐酸,产生CO2的体积与所加盐酸体积之间关系如图所示.下列判断正确的是( )| A. | 原NaOH溶液的浓度为0.2 mol•L-1 | |
| B. | B烧杯中通入的CO2体积为448 mL | |
| C. | 通入CO2后,不能确定A烧杯中的溶质 | |
| D. | 通入CO2后,C烧杯中溶质成分为NaOH和 Na2CO3,且物质的量相等 |
5.1mol 下列物质与足量的NaOH溶液充分反应,消耗的NaOH的物质的量为( )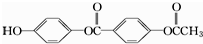

| A. | 3 mol | B. | 4mol | C. | 5 mol | D. | 6 mol |
15.下列叙述中正确的是( )
| A. | 硝酸的摩尔质量是63 g | |
| B. | 1 mol CO的质量是28 g | |
| C. | 4 g氢气对应的摩尔质量是2 g氢气对应的摩尔质量的2倍 | |
| D. | 铁的摩尔质量在数值上等于铁原子的相对原子质量 |
2.某化工厂以丙烯、乙烯为原料进行化工生产的主要流程如图.下列有关说法错误的是( )
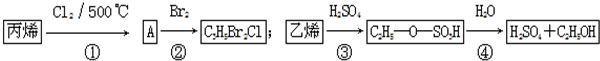
其中①CH3-CH=CH2+Cl2$\stackrel{500℃}{→}$Cl-CH2-CH=CH2+HCl.

其中①CH3-CH=CH2+Cl2$\stackrel{500℃}{→}$Cl-CH2-CH=CH2+HCl.
| A. | 反应①与反应④均是取代反应 | |
| B. | 反应②与反应③均是加成反应 | |
| C. | 反应②中产物的结构简式为CH2BrCH2CHClBr | |
| D. | 反应③、④表明硫酸是乙烯与水反应的催化剂 |
19.下述实验操作中,正确的是( )
| A. | 配置硫酸溶液时,将浓硫酸慢慢注入盛有水的容量瓶中进行配制 | |
| B. | 用托盘天平称量8.75g NaCl固体 | |
| C. | 将混合液蒸馏分离时,应使温度计水银球浸没在混合液中 | |
| D. | 分液时,将上层液体从分液漏斗上口倒出,下层液体从分液漏斗下口放出 |
20.下列描述涉及化学变化的是( )
| A. | 山崩地裂 | B. | 百炼成钢 | C. | 木已成舟 | D. | 花香四溢 |