题目内容
根据下列三个反应的化学方程式:I2+SO2+2H2O=H2SO4+2HI;2FeCl2+Cl2=2FeCl3;2FeCl3+2HI=2FeCl2+2HCl+I2,判断在FeI2与H2SO3的混合溶液中通入少量的Cl2,一定发生的反应( )
| A、Cl2+2I-=2Cl-+I2 |
| B、Cl2+2Fe2+=2Fe3++2Cl- |
| C、Cl2+H2SO3+H2O═4H++SO42-+2Cl- |
| D、2FeI2+3Cl2=2FeCl3+2I2 |
考点:氯气的化学性质,铁盐和亚铁盐的相互转变
专题:元素及其化合物
分析:由氧化剂的氧化性大于氧化产物的氧化性可知,氧化性为Cl2>Fe3+>I2>H2SO4,结合发生的反应判断.
解答:
解:由已知反应可知,氧化性为Cl2>Fe3+>I2>H2SO4,则还原性为SO2>I->Fe2+>Cl-,
FeI2与H2SO3的混合溶液中通入少量的Cl2,只有还原性最强的H2SO3先被氧化,则发生的离子反应为Cl2+H2SO3+H2O═4H++SO42-+2Cl-,
故选C.
FeI2与H2SO3的混合溶液中通入少量的Cl2,只有还原性最强的H2SO3先被氧化,则发生的离子反应为Cl2+H2SO3+H2O═4H++SO42-+2Cl-,
故选C.
点评:本题考查氧化还原反应及氯气的性质,为高频考点,把握还原性的强弱及优先氧化的分析为解答的关键,注意氯气少量,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列有关实验操作正确的是( )
A、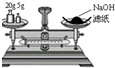 称量氢氧化钠固体 |
B、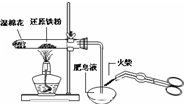 检验铁粉与水蒸气反应产生的氢气 |
C、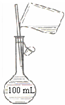 配制150 mL 0.10 mol/L盐酸 |
D、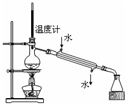 分离两种互溶但沸点相差较大的液体混合物 |
相同温度下,体积均为1.5L的两个恒容容器中发生可逆反应:
X2(g)+3Y2(g)?2XY3(g)△H=-92.6kJ?mol-1,实验测得有关数据如表:
下列叙述不正确的是( )
X2(g)+3Y2(g)?2XY3(g)△H=-92.6kJ?mol-1,实验测得有关数据如表:
| 容器编号 | 起始时各物质物质的量/mol | 达平衡时体系能量的变化 | ||
| X2 | Y2 | XY3 | ||
| ① | 1 | 3 | 0 | 放热46.3kJ |
| ② | 0.8 | 2.4 | 0.4 | Q(Q>0) |
| A、容器①中达到平衡时,Y2的转化率为50% |
| B、Q=27.78kJ |
| C、若X2、Y2、XY3改按0、0、2投料,则达到平衡时吸热46.3KJ |
| D、若容器①体积改为1.0L.则达平衡时放出的热量小于46.3kJ |
将钠加入到下列溶液中,既产生气体又产生沉淀的是( )
| A、CuCl2 |
| B、Na2SO4 |
| C、MgCl2 |
| D、KNO3 |
下列说法正确的是( )
| A、放热的反应在常温下一定易进行 |
| B、吸热反应在常温下不能进行 |
| C、有吸热或放热现象的过程中一定发生了化学反应 |
| D、反应是放热还是吸热是由反应物和生成物所具有的能量的相对大小决定的 |
下列食品添加剂与类别对应正确的一组是( )
| A、着色剂-----醋酸 |
| B、疏松剂-----碳酸氢钠 |
| C、调味剂------亚硝酸钠 |
| D、防腐剂------苯甲酸钠 |
人体正常血红蛋白中含有Fe2+,若误食亚硝酸盐,会导致Fe2+转化为Fe3+而中毒,服用维生素C可以解毒.对上述事实分析不正确的是( )
| A、亚硝酸盐是氧化剂 |
| B、维生素C是氧化剂 |
| C、亚硝酸盐将Fe3+还原成Fe2+ |
| D、维生素C被Fe3+氧化 |
设nA为阿伏加德罗常数的数值,下列说法正确的是( )
| A、常温下,23g NO2 含有nA个氧原子 |
| B、0.1mol/L NaCl溶液含有0.1nA个Cl- |
| C、常温常压下,22.4L CCl4含有nA个CCl4分子 |
| D、含NA个Na+的Na2O溶解于1 L水中,Na+的物质的量浓度为1mol/L |
下列能达到实验目的是( )
A、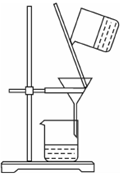 除去Fe(OH)3胶体中的FeCl3 |
B、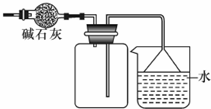 干燥、收集氨气,并吸收多余的氨气 |
C、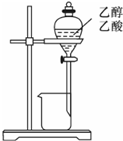 分离乙醇、乙酸 |
D、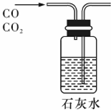 除去杂质气体二氧化碳 |