题目内容
工业生产粗硅的主要原理为:SiO2+(1)若在制粗硅的过程中同时生成了碳化硅,且生成的硅和碳化硅的物质的量之比为5∶1,则参加反应的C和SiO2的质量比为____________。
(2)工业上可通过如下流程由粗硅制取纯硅:
Si(粗)![]() SiCl4(l)
SiCl4(l) ![]() Si(纯)
Si(纯)
若上述反应中Si(粗)和SiCl4的利用率均为80%,制粗硅时有10%的SiO2转化为SiC,则生产100.8 t纯硅需纯度为75%的石英砂多少吨?
(3)工业上还可以通过下图所示的流程来制取纯硅:

反应①:Si(粗)+3HCl(g) ![]() SiHCl3(l)+H2(g)
SiHCl3(l)+H2(g)
反应②:SiHCl3+H2![]() Si(纯)+3HCl
Si(纯)+3HCl
假设在每一轮次的投料生产中,硅元素没有损失,反应①中HCl的利用率为75%,反应②中H2的利用率为80%,则在下轮次的生产中,需补充投入HCl和H2的体积比为多少?
(1)13∶30
(2)设需纯度为75%的石英砂的质量为x。
根据题意有下列关系式:
SiO2 — Si — SiCl4 — Si(纯)
60 28
x×75%×(1-10%)×80%×80% 100.8 t
解得:x=500 t
(3)设每轮生产投入的粗硅中含1 mol Si,
则由反应①可知:消耗HCl的物质的量为3 mol/75%=4 mol,生成H2的物质的量为1 mol。
由反应②可知:消耗H2的物质的量为1 mol/80%=1.25 mol,生成HCl的物质的量为3 mol。
则在一轮次的生产中,需补充投入HCl和H2的物质的量之比(即体积比)为:
(4 mol-3 mol)∶(1.25 mol-1 mol)=4∶1
解析:本题考查化学计算的能力。
(1)SiO2+![]() Si+2CO↑ Si+C
Si+2CO↑ Si+C![]() SiC
SiC
当生成的硅和碳化硅的物质的量之比为5∶1时,参加反应的C和SiO2的物质的量之比为13∶6。
(2)设需纯度为75%的石英砂x。根据题意有下列关系式:
SiO2 — Si — SiCl4 — Si(纯)
60 28
x×75%×(1-10%)×80%×80% 100.8 t
解得:x=500 t
或由Si原子守恒:x×75%×(1-10%)×80%×80%/60=100.8/28
解得:x=500 t
(3)设每轮生产投入的粗硅中含1 mol Si。则由反应①可知:消耗HCl的物质的量为3 mol/75%=4 mol,生成H2的物质的量为1 mol。由反应②可知:消耗H2的物质的量为1 mol/80%=1.25 mol,生成HCl的物质的量为3 mol。则在一轮次的生产中,需补充投入HCl和H2的物质的量之比(即体积比)为(4 mol-3 mol)∶(1.25 mol-1 mol)=4∶1。

 轻巧夺冠周测月考直通中考系列答案
轻巧夺冠周测月考直通中考系列答案工业生产粗硅的主要原理为:SiO2+2C 3273K Si(粗)+2CO↑。
(1)若在制粗硅的过程中同时生成了碳化硅,且生成的硅和碳化硅的物质的量之比为5∶1,则参加反应的C和SiO2的质量比为 ?? 。
(2)工业上可通过如下流程由粗硅制取纯硅:
| ||||||
|
| |||||
![]()
![]()
![]() Si(粗) SiCl4(l) Si(纯)
Si(粗) SiCl4(l) Si(纯)
若上述反应中Si(粗)和SiCl4的利用率均为80%,制粗硅时有10%的SiO2转化为SiC,则生产100.8t纯硅需纯度为75%的石英砂多少吨?
(3)工业上还可以通过下图所示的流程来制取纯硅:
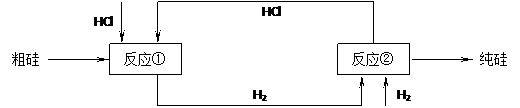
反应①: Si(粗)+3HCl(g) 553~573K SiHCl3(l)+H2(g)
反应②: SiHCl3+H2 1373K Si(纯)+3HCl
假设在每一轮次的投料生产中,硅元素没有损失,反应①中HCl的利用率为75%,反应②中H2的利用率为80%,则在下轮次的生产中,需补充投入HCl和H2的体积比为多少?


 2CO↑+Si
2CO↑+Si