题目内容
3.现有部分短周期主族元素的性质或原子结构如表:| 元素编号 | 元素性质或原子结构 |
| T | M层上有6个电子 |
| W | 短周期内原子半径最大的元素 |
| N | 原子序数比T小,且与T在同一主族 |
| X | 最外层电子数是次外层电子数的2倍 |
| Y | 常温下单质为双原子分子,其氨化物的水溶液呈碱性 |
| Z | 元素最高正价为+7价 |
(2)XN2的电子式是:
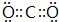 ,Y的简单氢化物的结构式
,Y的简单氢化物的结构式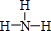 .
.(3)在最高价氧化物的水化物中,酸性最强的化合物的分子式是HClO4.
(4)用电子式表示WZ的形成过程
 .
.(5)元素Z和T相比,非金属性较强的是Cl(用元素符号表示),下列表述中能证明这一事实的是B.
A.常温下Z单质和T单质状态不同B.Z的氢化物比T的氢化物稳定
C.一定条件下,Z和T的单质都能与氢氧化钠溶液反应
(6)写出W单质和H2O反应的化学方程式2Na+2H2O=2NaOH+H2↑所得溶液的溶质是离子化合物(填“离子”或“共价”).
分析 短周期主族元素中,T元素原子M层上有6个电子,则T为S元素;W是短周期内原子半径最大的元素,则W为Na;N的原子序数比T(硫)小,且与T在同一主族,则N为O元素;X元素原子最外层电子数是次外层电子数的2倍,则X原子只能有2个电子层,最外层电子数为4,则X为C元素;常温下Y元素单质为双原子分子,其氢化物水溶液呈碱性,则Y为N元素;Z元素最高正价是+7价,则Z为Cl元素,据此解答.
解答 解:短周期主族元素中,T元素原子M层上有6个电子,则T为S元素;W是短周期内原子半径最大的元素,则W为Na;N的原子序数比T(硫)小,且与T在同一主族,则N为O元素;X元素原子最外层电子数是次外层电子数的2倍,则X原子只能有2个电子层,最外层电子数为4,则X为C元素;常温下Y元素单质为双原子分子,其氢化物水溶液呈碱性,则Y为N元素;Z元素最高正价是+7价,则Z为Cl元素.
(1)元素Y为N元素,在周期表中的位置:第二周期第ⅤA族,
故答案为:第二周期第ⅤA族;
(2)CO2的电子式是: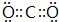 ,Y的简单氢化物为NH3,结构式为
,Y的简单氢化物为NH3,结构式为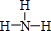 ,
,
故答案为: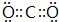 ;
;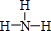 ;
;
(3)在最高价氧化物的水化物中,酸性最强的化合物的分子式是:HClO4,
故答案为:HClO4;
(4)用电子式表示NaCl的形成过程: ,
,
故答案为: ;
;
(5)同周期自左而右元素非金属性增强,故非金属性较强的是Cl,
A.单质的状态属于物理性质,不能比较非金属性强弱,故A错误;
B.非金属性与氢化物稳定性一致,氯的氢化物比硫的氢化物稳定,说明Cl元素非金属性更强,故B正确;
C.非金属单质与氢氧化钠溶液反应不能判断非金属性强弱,如氧气不与氢氧化钠溶液反应,而硫可以,故C错误.
故答案为:Cl;B;
(6)Na单质和H2O反应的化学方程式:2Na+2H2O=2NaOH+H2↑,所得溶液的溶质是NaOH,属于离子化合物,
故答案为:2Na+2H2O=2NaOH+H2↑;离子.
点评 本题考查结构性质位置关系应用,注意掌握金属性、非金属性强弱比较实验事实,有利于基础知识的巩固.

| 元素编号 | 元素性质或原子结构 |
| T | M层电子数是K层电子数的3倍 |
| X | 一种同位素可测定文物年代 |
| Y | 常温下单质为双原子分子,其氢化物水溶液呈碱性 |
| Z | 元素最高正价是+7价 |
(2)元素Z在周期表中的位置为第三周期ⅦA族.Y单质的结构式为N≡N.
(3)元素Y与氢元素形成一种离子YH4+,实验室检验溶液中含有这种离子方法是:NH4++OH-$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O(仅用离子反应方程式表示).
(4)元素Z与元素T相比,非金属性较强的是Cl(用元素符号表示),下列表述中能证明这一事实的是bd.
a.常温下Z的单质和T的单质状态不同
b.Z的氢化物比T的氢化物稳定
c.一定条件下Z和T的单质都能与氢氧化钠溶液反应
d.Z的最高价氧化物对应水化物的酸性比T的最高价氧化物对应水化物的酸性强.
| A. | 浓硫酸稀释时溶液温度升高,说明浓硫酸稀释只有水合过程 | |
| B. | 蔗糖是非电解质,放入水中溶液温度没有明显变化,说明蔗糖溶于水既没有扩散过程也没有水合过程 | |
| C. | 家用石碱(Na2CO3•10H2O)久置后,由块状变成粉末状,这一变化是风化的结果 | |
| D. | 从冰箱中取出物品,表面很快出现水珠,这种现象叫潮解 |
| A. | 室温下CH3COONa溶液的pH值大于7 | |
| B. | 同温同浓度的盐酸与CH3COOH溶液比较,醋酸溶液导电能力弱 | |
| C. | CH3COOH不与NaCl反应 | |
| D. | 室温下0.1 mol/L CH3COOH溶液的pH=2.9 |
根据以上方程式,下列推论正确的是( )
| A. | 当lmol白磷转变成红磷时放出17kJ热量 | |
| B. | 当4g红磷转变成白磷时吸收17kJ热量 | |
| C. | 正反应是一个放热反应 | |
| D. | 白磷热稳定性比红磷大 |
| 元素编号 | 元素性质与原子(或分子)结构 |
| T | 最外层电子数是次外层电子数的 3 倍 |
| X | 常温下单质为双原子分子,分子中含有 3 对共用电子对 |
| Y | M 层比 K 层少 1 个电子 |
| Z | 第 3 周期元素的简单离子中半径最小 |
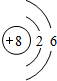
(2)元素 Y 与元素 Z 相比,金属性较强的是Na(用元素符号表示),下列表述中能证明这一事实的是CD(填序号).
A.Y 单质的熔点比 Z 单质低 B.Y 的化合价比 Z 低
C.Y 单质与水反应比 Z 单质剧烈 D.Y 最高价氧化物的水化物的碱性比 Z 强
(3)X 元素的气态氢化物与其最高价含氧酸反应的离子方程式为NH3+H+=NH4+.
(4)元素 T 和氢元素以原子个数比 1:1 化合形成化合物 Q,元素 X 与氢元素以原子个数比 1:2 化合形成常用作火箭燃料的化合物 W,Q 与 W 发生氧化还原反应,生成 X 单质和 T 的另一种氢化物,写出该反应的化学方程式2H2O2+N2H4=4H2O+N2↑.
| A. | pH=12的Ba(OH)2溶液和pH=12的Na2CO3溶液中,水电离的c(H+)相等 | |
| B. | 常温下,pH=4的醋酸与pH=10的NaOH溶液等体积混合后pH<7 | |
| C. | 将0.2 mol•L-1NaA溶液和0.1 mol•L-1盐酸溶液等体积混合所得碱性溶液中:c(Na+)+c(H+)=c(A-)+c(Cl-) | |
| D. | 0.1 mol•L-1 Na2CO3溶液中:c(Na+)=c(HCO${\;}_{3}^{-}$)+c(H2CO3)+2c(CO${\;}_{3}^{2-}$) |
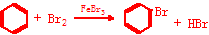 .
.