题目内容
14.将2.3g的钠用足量大的没被氧化的铝箔包住,铝箔上用针扎些小孔放入足量的水中,写出有关反应的化学方程式,产生的氢气在标态下体积是多少升?分析 发生反应的方程式为:2Na+2H2O=2NaOH+H2↑、2Al+2NaOH+2H2O=2NaAlO2+3H2↑,根据n=$\frac{m}{M}$计算出钠的物质的量,然后结合反应方程式计算出生成氢气的物质的量,最后根据V=nVm计算出生成氢气在标准状况下的体积.
解答 解:发生反应的化学方程式有:2Na+2H2O=2NaOH+H2↑、2Al+2NaOH+2H2O=2NaAlO2+3H2↑,
2.3gNa的物质的量为:$\frac{2.3g}{23g/mol}$=0.1mol,
根据反应2Na+2H2O=2NaOH+H2↑可知,0.1molNa完全反应生成氢气的物质的量为:n(H2)=0.1mol×$\frac{1}{2}$=0.05mol,同时反应生成0.1molNaOH,
铝足量,根据反应 2Al+2NaOH+2H2O=2NaAlO2+3H2↑可知生成氢气的物质的量为:n(H2)=0.1mol×$\frac{3}{2}$=0.15mol,
反应生成氢气的总物质的量为:0.05mol+0.15mol=0.2mol,
标准状况下0.2mol氢气的体积为:22.4L/mol×0.2mol=4.48L,
答:发生反应的化学方程式有:2Na+2H2O=2NaOH+H2↑、2Al+2NaOH+2H2O=2NaAlO2+3H2↑,反应生成氢气在标准状况下的体积为4.48L.
点评 本题考查了化学方程式的计算,题目难度中等,明确发生反应的原理为解答关键,注意掌握物质的量与摩尔质量、气体摩尔体积之间的关系,试题培养了学生的化学计算能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
5.某溶液中有Ba2+、Mg2+、Ag+,现用①KOH溶液,②K2SO4溶液,③KCl溶液,将三种离子逐一沉淀并分离的过程中,用到的分离方法及次数分别是( )
| A. | 洗涤,2次 | B. | 过滤,2次 | C. | 分液,3次 | D. | 过滤,3次 |
2.下列有机反应属于加成反应的是( )
| A. | CH4+Cl2 $\stackrel{光照}{→}$ CH3Cl+HCl | B. | CH2═CH2+Br2→CH2BrCH2Br | ||
| C. | 2CH3CH2OH+O2$→_{△}^{Cu}$2CH3CHO+2H2O | D. | 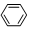 +HNO3$→_{50~60℃}^{浓H_{2}SO_{4}}$ +HNO3$→_{50~60℃}^{浓H_{2}SO_{4}}$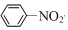 +H2O +H2O |
9.下列实验操作能达到实验目的是( )
| 实验目的 | 实验操作 | |
| A | 实验室制大量CO2 | 向石灰石中加入稀硫酸 |
| B | 证明某溶液中含有SO42- | 向该溶液中滴入BaCl2溶液 |
| C | 配制0.1mol/L CuSO4溶液 | 把2.5g胆矾晶体溶于水配成100mL溶液 |
| D | 制备Fe(OH)3胶体 | 将饱和的FeCl3溶液滴加到热NaOH溶液中 |
| A. | A | B. | B | C. | C | D. | D |
19.下列事实与胶体的性质无关的是( )
| A. | “尿毒症”患者做血液透析治疗 | |
| B. | FeCl3溶液中滴入NaOH溶液出现红褐色沉淀 | |
| C. | 在河流入海处易形成沙洲 | |
| D. | 在豆浆中加入盐卤制豆腐 |
6.现有常温下的四种溶液(如表),下列有关叙述正确的是( )
| ① | ② | ③ | ④ | |
| 氨水 | 氢氧化钠 | 醋酸 | 盐酸 | |
| pH | 11 | 11 | 3 | 3 |
| A. | 分别加水稀释10倍,四种溶液的pH为:①>②>③>④ | |
| B. | 温度上升10℃,四种溶液的pH不变 | |
| C. | ③④中分别加入适量的氯化按晶体后,③的pH减小,④的pH不变 | |
| D. | 将①④两种溶液等体积混合,所得溶液中c (C1-)>c NH4+)>c (H+)>c (OH-) |
4.现有以下混合液体:
①汽油和氯化钠溶液 ②乙醇与水 ③氯化钠溶液和单质溴,分离以上各混合液的正确方法依次是( )
①汽油和氯化钠溶液 ②乙醇与水 ③氯化钠溶液和单质溴,分离以上各混合液的正确方法依次是( )
| A. | 分液、萃取、蒸馏 | B. | 萃取、蒸馏、分液 | C. | 分液、蒸馏、萃取 | D. | 蒸馏、萃取、分液 |

 .
. .
.