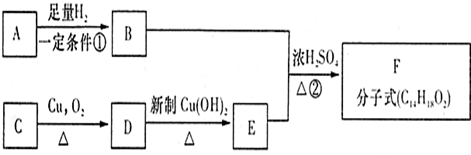
题目内容
对某氯化物溶液进行如图所示实验
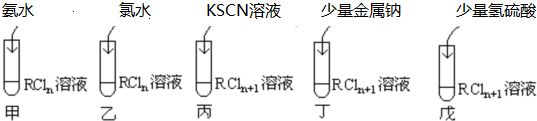
(1)甲中现象 化学方程式
(2)乙中现象 离子方程式
(3)丙中现象 离子方程式
(4)丁中现象 离子方程式
(5)戊中现象 离子方程式 .

(1)甲中现象
(2)乙中现象
(3)丙中现象
(4)丁中现象
(5)戊中现象
考点:离子方程式的书写
专题:
分析:由实验可知,R为变价金属,能与KSCN溶液反应,能与H2S反应,则R为Fe,n=2,
(1)氯化亚铁与氨水反应生成氢氧化亚铁沉淀;
(2)氯化亚铁与氯水反应生成氯化铁;
(3)铁离子与KSCN结合生成络离子;
(4)水与Na反应生成氢气,NaOH与铁离子反应生成沉淀;
(5)氯化铁与H2S反应生成亚铁离子、S.
(1)氯化亚铁与氨水反应生成氢氧化亚铁沉淀;
(2)氯化亚铁与氯水反应生成氯化铁;
(3)铁离子与KSCN结合生成络离子;
(4)水与Na反应生成氢气,NaOH与铁离子反应生成沉淀;
(5)氯化铁与H2S反应生成亚铁离子、S.
解答:
解:由实验可知,R为变价金属,能与KSCN溶液反应,能与H2S反应,则R为Fe,n=2,
(1)氯化亚铁与氨水反应生成氢氧化亚铁沉淀,观察到白色沉淀迅速变为灰绿色最后变为红褐色,发生的化学反应为FeCl2+2NH3.H2O=Fe(OH)2↓+2NH4Cl、4Fe(OH)2+O2+2H2O=4Fe(OH)3,故答案为:白色沉淀迅速变为灰绿色最后变为红褐色;FeCl2+2NH3.H2O=Fe(OH)2↓+2NH4Cl、4Fe(OH)2+O2+2H2O=4Fe(OH)3;
(2)氯化亚铁与氯水反应生成氯化铁,观察到浅绿色溶液变为棕黄色溶液,离子反应为2Fe2++Cl2=2Fe3++2Cl-,故答案为:浅绿色溶液变为棕黄色溶液;2Fe2++Cl2=2Fe3++2Cl-;
(3)铁离子与KSCN结合生成络离子,观察到溶液为血红色,离子反应为Fe3++3SCN-=Fe(SCN)3,故答案为:溶液为血红色;Fe3++3SCN-=Fe(SCN)3;
(4)观察到有无色气体生成,并有红褐色沉淀生成,发生的离子反应为2Na+2H2O=2Na++2OH-+H2↑、Fe3++3OH-=Fe(OH)3↓,故答案为:有无色气体生成,并有红褐色沉淀生成;2Na+2H2O=2Na++2OH-+H2↑、Fe3++3OH-=Fe(OH)3↓;
(5)氯化铁与H2S反应生成氯化亚铁、S,观察到溶液变浑浊有淡黄色沉淀生成,溶液为浅绿色,发生的离子反应为2Fe3++H2S=2Fe2++S↓+2H+,故答案为:溶液变浑浊有淡黄色沉淀生成,溶液为浅绿色;2Fe3++H2S=2Fe2++S↓+2H+.
(1)氯化亚铁与氨水反应生成氢氧化亚铁沉淀,观察到白色沉淀迅速变为灰绿色最后变为红褐色,发生的化学反应为FeCl2+2NH3.H2O=Fe(OH)2↓+2NH4Cl、4Fe(OH)2+O2+2H2O=4Fe(OH)3,故答案为:白色沉淀迅速变为灰绿色最后变为红褐色;FeCl2+2NH3.H2O=Fe(OH)2↓+2NH4Cl、4Fe(OH)2+O2+2H2O=4Fe(OH)3;
(2)氯化亚铁与氯水反应生成氯化铁,观察到浅绿色溶液变为棕黄色溶液,离子反应为2Fe2++Cl2=2Fe3++2Cl-,故答案为:浅绿色溶液变为棕黄色溶液;2Fe2++Cl2=2Fe3++2Cl-;
(3)铁离子与KSCN结合生成络离子,观察到溶液为血红色,离子反应为Fe3++3SCN-=Fe(SCN)3,故答案为:溶液为血红色;Fe3++3SCN-=Fe(SCN)3;
(4)观察到有无色气体生成,并有红褐色沉淀生成,发生的离子反应为2Na+2H2O=2Na++2OH-+H2↑、Fe3++3OH-=Fe(OH)3↓,故答案为:有无色气体生成,并有红褐色沉淀生成;2Na+2H2O=2Na++2OH-+H2↑、Fe3++3OH-=Fe(OH)3↓;
(5)氯化铁与H2S反应生成氯化亚铁、S,观察到溶液变浑浊有淡黄色沉淀生成,溶液为浅绿色,发生的离子反应为2Fe3++H2S=2Fe2++S↓+2H+,故答案为:溶液变浑浊有淡黄色沉淀生成,溶液为浅绿色;2Fe3++H2S=2Fe2++S↓+2H+.
点评:本题考查离子反应方程式的书写及无机物的推断,为高频考点,把握变价金属铁及其化合物的性质为解答的关键,注意氧化还原反应及离子反应的综合分析,题目难度不大.

练习册系列答案
相关题目
诗句“春蚕到死丝方尽,蜡炬成灰泪始干”中的“丝”和“泪”分别是( )
| A、纤维素,脂肪 |
| B、蛋白质,高级烃 |
| C、淀粉,油脂 |
| D、蛋白质,硬化油 |
已知热化学方程式2H2(g)+O2(g)=2H2O(l)△H1<0;2H2O(g)=2H2(g)+O2(g)△H2.下列说法正确的是( )
| A、方程式中化学计量数表示分子数 |
| B、△H2>0 |
| C、△H2=-△H1 |
| D、利用△H1,△H2可求出水的气化热 |
下列离子方程式书写正确的是( )
| A、钠和水反应:2Na+2H2O═2Na++2OH-+H2↑ |
| B、FeCl3溶液腐蚀铜线路板:Cu+Fe3+═Cu2++Fe2+ |
| C、铜和浓HNO3反应:3Cu+8H++2NO3-═3Cu2++2NO2↑+4H2O |
| D、NaHSO4溶液与Ba(OH)2溶液反应至中性:H++SO42-+Ba2++OH-═BaSO4↓+H2O |
按“单质、氧化物、盐”的顺序排列的一组物质是( )
| A、SO2 S Na2SO4 |
| B、Si SiO2 Na2SiO3 |
| C、CO2 Na2CO3 C |
| D、Al Al2O3 Al(OH)3 |

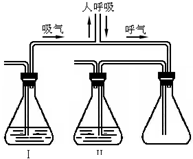 某化学兴趣小组为了证明人呼出的气体中含有CO2,设计了如图所示的实验装置.你认为锥形瓶Ⅰ、Ⅱ中应选用的一组试剂是( )
某化学兴趣小组为了证明人呼出的气体中含有CO2,设计了如图所示的实验装置.你认为锥形瓶Ⅰ、Ⅱ中应选用的一组试剂是( )