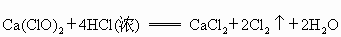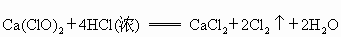题目内容
已知漂白粉与浓盐酸在常温下即可反应生成氯气:
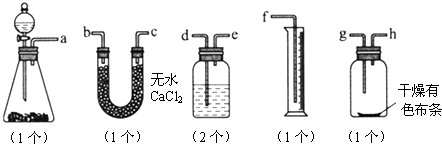
Ca(ClO)2+4HCl(浓)常温下,氯气在水中溶解度较大,但在饱和食盐水中溶解度很小.某同学为了测定产生氯气的体积并验证干燥而纯净的氯气无漂白性,用图所示的实验装置进行实验.回答下列问题:
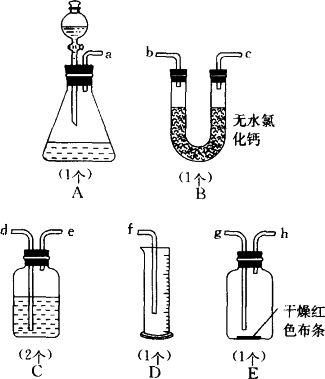
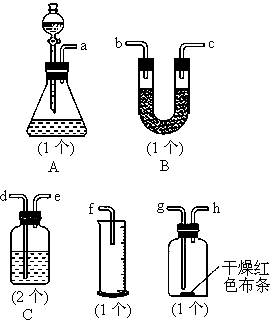
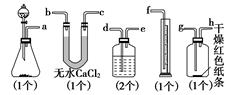
(1)请用字母填写装置的连接顺序:a接( )、( )接( )、( )接( )、( )接( )、( )接( );
(2)洗气瓶中所装液体是________;
(3)在制氯气前,必须进行的一项操作步骤是________;
(4)某同学在实验中发现量筒中未收集到液体,则失败的原因可能是________、________、________.
答案:
解析:
提示:
解析:
答案:(1)d e b c g h e d f或d e c b g h e d f
(2)饱和食盐水
(3)检查装置的气密性
(4)装置漏气 盐酸过稀 e与f连接
解析:本题要得到干燥纯净的氯气并测定其性质和体积.按装置串联的一般顺序:发生装置→净化装置→性质验证装置→尾气处理装置,本题发生装置为A,净化装置为C(饱和食盐水除HCl气体)和B(除H2O),性质验证装置为E,气体体积测量装置为C和D.
提示:
该题紧扣知识点“实验室利用化学反应制取氯气”.具体内容涉及制取氯气的化学原理、氯气的净化与收集原理、氯气的性质及应用、简单的实验设计与评价,属于多项基础知识和基本技能综合型题.

练习册系列答案
相关题目