题目内容
 化学在环境保护中起着十分重要的作用.催化反硝化法和电化学降解法可用于治理水中硝酸盐的污染.
化学在环境保护中起着十分重要的作用.催化反硝化法和电化学降解法可用于治理水中硝酸盐的污染.(1)催化反硝化法中,H2能将NO3-还原为N2.25℃时,反应进行10min,溶液的pH由7变为12.
①N2的电子式为
②上述反应离子方程式为
其平均反应速率v(NO3-)为
③还原过程中可生成中间产物NO2-,写出3种促进NO2-水解的方法
(2)电化学降解NO3-的原理如图所示.电源正极为
考点:原电池和电解池的工作原理
专题:电化学专题
分析:(1)①氮气分子中氮原子间存在3个共用电子对;
②在催化剂条件下,氢气和硝酸根离子发生氧化还原反应生成氮气、水和氢氧根离子;先根据溶液pH的变化计算氢氧根离子反应速率,再根据氢氧根离子和硝酸根离子之间的关系式计算硝酸根离子反应速率;
③亚硝酸根离子水解是吸热反应,根据外界条件对其水解反应影响来分析;
(2)①由图示知在Ag-Pt电极上NO3-发生还原反应,因此Ag-Pt电极为阴极,则B为负极,A为电源正极;在阴极反应是NO3-得电子发生还原反应生成N2,利用电荷守恒与原子守恒知有氢离子参与反应且有水生成.
②在催化剂条件下,氢气和硝酸根离子发生氧化还原反应生成氮气、水和氢氧根离子;先根据溶液pH的变化计算氢氧根离子反应速率,再根据氢氧根离子和硝酸根离子之间的关系式计算硝酸根离子反应速率;
③亚硝酸根离子水解是吸热反应,根据外界条件对其水解反应影响来分析;
(2)①由图示知在Ag-Pt电极上NO3-发生还原反应,因此Ag-Pt电极为阴极,则B为负极,A为电源正极;在阴极反应是NO3-得电子发生还原反应生成N2,利用电荷守恒与原子守恒知有氢离子参与反应且有水生成.
解答:
解:(1)①N2分子中氮原子间通过氮氮三键结合,且每个N原子含有一对孤电子对,因此其电子式为 ,
,
故答案为: ;
;
②利用溶液pH变化可知有OH-生成,再结合原子守恒可写出反应的离子方程式为:
2NO3-+5H2=N2+2OH-+4H2O,利用离子方程式知v(NO3-)=v(OH-)=
mol/(L?min)=0.001 mol/(L?min),
故答案为:2NO3-+5H2=N2+2OH-+4H2O,0.001;
③亚硝酸盐水解是吸热反应,且水解时生成氢氧根离子,稀释亚硝酸盐溶液能促进其水解,所以要使NO2-水解使溶液中c(OH-)变大,可促进NO2-水解的措施有加热、加水或加酸等,故答案为:加水、升高温度、加酸;
(2)由图示知在Ag-Pt电极上NO3-发生还原反应,因此Ag-Pt电极为阴极,则B为负极,A为电源正极;在阴极反应是NO3-得电子发生还原反应生成N2,利用电荷守恒与原子守恒知有H2O参与反应且有水生成,
所以阴极上发生的电极反应式为:2NO3-+12H++10e-=N2+6H2O,
故答案为:A,2NO3-+12H++10e-=N2+6H2O.
 ,
,故答案为:
 ;
;②利用溶液pH变化可知有OH-生成,再结合原子守恒可写出反应的离子方程式为:
2NO3-+5H2=N2+2OH-+4H2O,利用离子方程式知v(NO3-)=v(OH-)=
| 10-2-10-7 |
| 10 |
故答案为:2NO3-+5H2=N2+2OH-+4H2O,0.001;
③亚硝酸盐水解是吸热反应,且水解时生成氢氧根离子,稀释亚硝酸盐溶液能促进其水解,所以要使NO2-水解使溶液中c(OH-)变大,可促进NO2-水解的措施有加热、加水或加酸等,故答案为:加水、升高温度、加酸;
(2)由图示知在Ag-Pt电极上NO3-发生还原反应,因此Ag-Pt电极为阴极,则B为负极,A为电源正极;在阴极反应是NO3-得电子发生还原反应生成N2,利用电荷守恒与原子守恒知有H2O参与反应且有水生成,
所以阴极上发生的电极反应式为:2NO3-+12H++10e-=N2+6H2O,
故答案为:A,2NO3-+12H++10e-=N2+6H2O.
点评:本题考查了氧化还原反应、原电池原理,根据元素化合价变化分析解答氧化还原反应,根据图象中微粒变化确定正负极上发生的反应,难点是电极反应式的书写,题目难度中等.

练习册系列答案
 鸿图图书寒假作业假期作业吉林大学出版社系列答案
鸿图图书寒假作业假期作业吉林大学出版社系列答案
相关题目
有机物的分子中,当它含有下列的一种官能团时,既能发生取代反应,氧化反应,酯化反应,又能发生消去反应的是( )
| A、-COOH |
B、 |
| C、-OH |
D、 |
 (1)硼酸(H3BO3)溶液中存在如下平衡:
(1)硼酸(H3BO3)溶液中存在如下平衡: A、B、C三种短周期元素在周期表中相对位置如表格:
A、B、C三种短周期元素在周期表中相对位置如表格: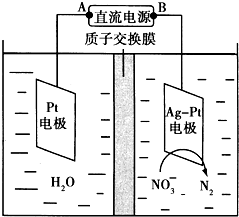 化学在环境保护中起着十分重要的作用.催化反硝化法和电化学降解法可用于治理水中硝酸盐的污染.
化学在环境保护中起着十分重要的作用.催化反硝化法和电化学降解法可用于治理水中硝酸盐的污染. 某实验小组依据甲醇燃烧的反应原理,设计如图所示的电池装置.
某实验小组依据甲醇燃烧的反应原理,设计如图所示的电池装置.