题目内容
10.下列表示正确的是( )| A. | 乙烯的球棍模型: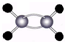 | B. | 镁的原子结构示意图: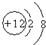 | ||
| C. | 氯化钠的电子式: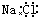 | D. | 乙炔的结构简式:CHCH |
分析 A.乙烯分子中含有1个碳碳双键,碳原子的原子半径大于氢原子;
B.镁原子的核电荷数=核外电子总数=12,最外层含有2个电子;
C.氯化钠为离子化合物,电子式中需要标出所带电荷;
D.乙炔分子中含有1个碳碳三键,结构简式中需要标出碳碳三键结构.
解答 解:A.乙烯分子中含有碳碳双键,碳原子的原子半径解答,乙烯的球棍模型为: ,故A正确;
,故A正确;
B.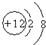 为镁离子结构示意图,镁原子的最外层含有2个电子,正确的原子结构示意图为:
为镁离子结构示意图,镁原子的最外层含有2个电子,正确的原子结构示意图为: ,故B错误;
,故B错误;
C.氯化钠是由钠离子和氯离子构成的,正确的电子式为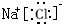 ,故C错误;
,故C错误;
D.乙炔分子中含有碳碳三键,正确的结构简式为:CH≡CH,故D错误;
故选A.
点评 本题考查了常见化学用语的表示方法,题目难度不大,涉及电子式、球棍模型、结构简式、原子结构示意图等知识,明确常见化学用语的书写原则为解答关键,试题培养了学生的规范答题能力.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
1.下列溶液中跟100mL 0.1mol/L 硫酸钾溶液里钾离子物质的量浓度相同的是( )
| A. | 100 mL 0.2 mol/L 氯化钾溶液 | B. | 200 mL 0.1 mol/L 硝酸钾溶液 | ||
| C. | 100 mL 0.1 mol/L 硝酸钾溶液 | D. | 50 mL 0.2 mol/L 磷酸钾溶液 |
18.X(g)+3Y(g)?2Z(g)△H=-a kJ•mol-1,一定条件下,将1mol X和3mol Y通入2L的恒容密闭容器中,反应10min,测得Y的物质的量为2.4mol.X的平均反应速率是( )
| A. | 0.03 mol•L-1•s-1 | B. | 0.03 mol•L-1•min-1 | ||
| C. | 0.01 mol•L-1•s-1 | D. | 0.01 mol•L-1•min-1 |
19.如图为元素周期表短周期中的一部分,有关元素X、Y、Z、M的说法错误的是( )
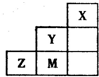

| A. | Y、Z可形成ZY6分子 | B. | X晶体属于原子晶体 | ||
| C. | 原子半径:Z>M>Y | D. | Z离子的结构示意图可表示为: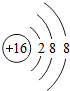 |
20.在标准状况下,进行甲、乙、丙三组实验:三组各取60mL同浓度盐酸溶液,加入同一种镁铝合金粉末,产生气体,有关数据列表如下:
则下列说法正确的是( )
| 实验序号 | 甲 | 乙 | 丙 |
| 合金质量/mg | 510 | 770 | 918 |
| 气体体积/mL | 560 | 672 | 672 |
| A. | 甲组和乙组的实验中,盐酸均是过量的 | |
| B. | 盐酸的物质的量浓度为0.8mol•L-1 | |
| C. | 合金中镁铝的物质的量之比为1:1 | |
| D. | 丙组中铝的物质的量为0.015mol |
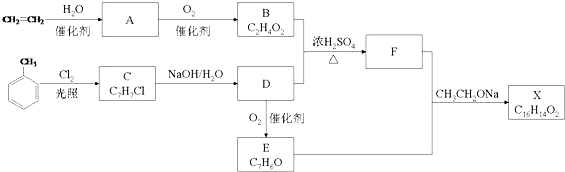

 +O2$→_{△}^{Cu}$2
+O2$→_{△}^{Cu}$2 +2H2O
+2H2O 
 B.
B.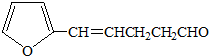
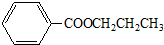
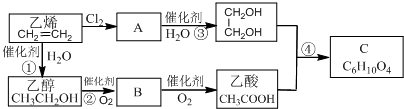
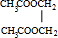 +2H2O.
+2H2O.
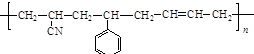 除苯乙烯外,还需要另外两种单体,写出这两种单体的结构简式CH2=CH-CN、CH2=CH-CH=CH2.
除苯乙烯外,还需要另外两种单体,写出这两种单体的结构简式CH2=CH-CN、CH2=CH-CH=CH2. )需要三步,第一步选用的试剂为HBr,目的是保护碳碳双键防止被加成.
)需要三步,第一步选用的试剂为HBr,目的是保护碳碳双键防止被加成.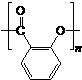 .
.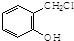 制备A的合成路线.
制备A的合成路线.