题目内容
5.将11.2L标准状况下的甲烷和某单烯羟的混合气体通入足量的溴的四氯化碳溶液中充分反应,溴的四氯化碳溶液增加了12.6g.该烯羟对氢气的相对密度为21(相对密度$\frac{ρ烯羟}{ρ氧气}$)①试确定该烯烃;
②求原混合气体中甲烷与烯烃的物质的量之比以及质量之比.
分析 该烯羟对氢气的相对密度为21,则相对分子质量为42,应为C3H6,为丙烯,丙烯与溴发生加成反应,溴的四氯化碳溶液增加的质量为丙烯的质量,计算混合气体、丙烯的物质的量,进而计算甲烷的物质的量,再计算甲烷的质量,以此解答该题.
解答 解:(1)该烯羟对氢气的相对密度为21,则相对分子质量为42,应为C3H6,为丙烯,
答:该烯烃为丙烯;
(2)丙烯与溴发生加成反应,溴的四氯化碳溶液增加的质量为12.6g,则:m(C3H6)=5.6g,n(C3H6)=$\frac{12.6g}{42g/mol}$=0.3mol,
而n(CH4)+n(C2H4)=$\frac{11.2L}{22.4L/mol}$=0.5mol,所以n(CH4)=0.5mol-0.3mol=0.2mol,故m(CH4)=0.2mol×16g/mol=3.2g,
故甲烷与烯烃的物质的量之比为0.2mol:0.3mol=2:3,
原混合气体中甲烷与乙烯的质量之比=3.2g:12.6g=16:63,
答:原混合气体中甲烷与烯烃的物质的量之比以及质量之比分别为2:3、16:63.
点评 本题考查混合物的计算,题目难度中等,明确甲烷和丙烯的性质差别是解题的关键,注意熟练掌握物质的量与摩尔质量、气体摩尔体积等物理量之间的转化关系.

练习册系列答案
 特高级教师点拨系列答案
特高级教师点拨系列答案
相关题目
15.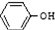 分子中苯环上的一个氢被-C3H7原子团取代形成的有机物共有( )
分子中苯环上的一个氢被-C3H7原子团取代形成的有机物共有( )
 分子中苯环上的一个氢被-C3H7原子团取代形成的有机物共有( )
分子中苯环上的一个氢被-C3H7原子团取代形成的有机物共有( )| A. | 6种 | B. | 8种 | C. | 10种 | D. | 12种 |
16.下列有关钠的叙述中错误的是( )
| A. | 电解法冶炼金属钠时,钠在阳极析出 | |
| B. | 钠的化学性质非常活泼,钠元素只能以化合态存在于自然界 | |
| C. | 钠的还原性很强,可以用来冶炼金属钛、锆、铌等 | |
| D. | 钠的质地软,可用小刀切割 |
13.进行下列实验时,仪器和药品选用都正确的是( )
| A. | 用饱和食盐水和电石在启普发生器中制乙炔 | |
| B. | 用氢氧化钠溶液洗去混在乙酸乙酯中的乙酸 | |
| C. | 把醋酸钠晶体与碱石灰混和,放在试管中加热制甲烷 | |
| D. | 苯和液溴混合于烧瓶中,加入铁粉制溴苯 |
20.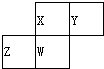 如图为元素周期表中短周期的一部分,四种元素均为非稀有气体元素.下列关于这四种元素及其化合物的说法中正确的是( )
如图为元素周期表中短周期的一部分,四种元素均为非稀有气体元素.下列关于这四种元素及其化合物的说法中正确的是( )
 如图为元素周期表中短周期的一部分,四种元素均为非稀有气体元素.下列关于这四种元素及其化合物的说法中正确的是( )
如图为元素周期表中短周期的一部分,四种元素均为非稀有气体元素.下列关于这四种元素及其化合物的说法中正确的是( )| A. | 原子半径:Z>W>X>Y | |
| B. | 气态氢化物的稳定性:Z>W>X>Y | |
| C. | W的最高正化合价与负化合价的绝对值不可能相等 | |
| D. | Z的最高价氧化物的水化物可能为强碱 |


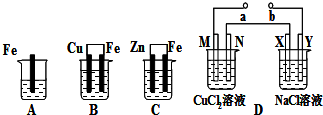
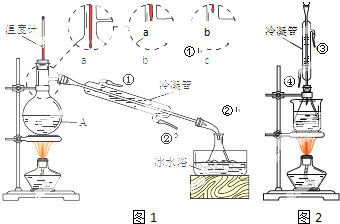 酒在酿造过程中部分醇会转化为羧酸,进而形成各种酯类化合物,使酒具有了特殊的香味.国家标准规定,优质高度浓香型白酒总酸量(以乙酸计)应不少于0.30g/L,总酯量(以乙酸乙酯计)应不少于2.0g/L.
酒在酿造过程中部分醇会转化为羧酸,进而形成各种酯类化合物,使酒具有了特殊的香味.国家标准规定,优质高度浓香型白酒总酸量(以乙酸计)应不少于0.30g/L,总酯量(以乙酸乙酯计)应不少于2.0g/L.