题目内容
诺贝尔物理学奖曾授予“光纤之父”英国华裔科学家高锟以及两位美国科学家威拉德·博伊尔和乔治·史密斯。光导纤维的主要成分是二氧化硅,下列关于二氧化硅的说法正确的是
A.二氧化硅是酸性氧化物,因此能与水反应生成硅酸
B.用二氧化硅制取单质硅时,当生成2.24 L气体(标准状况)时,得到2.8 g硅
C.二氧化硅制成的光导纤维,由于导电能力强而被用于制造光缆
D.二氧化硅不能与碳酸钠溶液反应,但能与碳酸钠固体在高温时发生反应
D
【解析】
试题分析:A.二氧化硅是酸性氧化物,由于SiO2不能溶于水,所以不能与水反应生成硅酸。错误。B.用二氧化硅制取单质硅的方程式为:SiO2+2C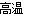 Si+2CO↑。若生成2.24 L气体(标准状况),即产生0.1mol的CO,根据方程式可知得到Si为0.05mol.即得到1.4g硅.错误。C.二氧化硅制成的光导纤维,是利用SiO2可以制成无色透明的“玻璃”,利用了该“玻璃”的全反射原理,传导光信号进行通信而被用于制造光缆。错误。D.由于酸性H2CO3>H2SiO3,所以在常温下二氧化硅不能与碳酸钠溶液反应,但是在高温下能与碳酸钠固体发生反应SiO2+ Na2CO3
Si+2CO↑。若生成2.24 L气体(标准状况),即产生0.1mol的CO,根据方程式可知得到Si为0.05mol.即得到1.4g硅.错误。C.二氧化硅制成的光导纤维,是利用SiO2可以制成无色透明的“玻璃”,利用了该“玻璃”的全反射原理,传导光信号进行通信而被用于制造光缆。错误。D.由于酸性H2CO3>H2SiO3,所以在常温下二氧化硅不能与碳酸钠溶液反应,但是在高温下能与碳酸钠固体发生反应SiO2+ Na2CO3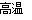 CO2↑+ Na2SiO3.这是利用高沸点的酸制取低沸点的酸。与溶液的酸性强弱无关。正确。
CO2↑+ Na2SiO3.这是利用高沸点的酸制取低沸点的酸。与溶液的酸性强弱无关。正确。
考点:考查二氧化硅的性质及应用的知识。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
 的值增大
的值增大 ΔH=+88.62 kJ/mol
ΔH=+88.62 kJ/mol

 R—COOH(R表示饱和烃基)
R—COOH(R表示饱和烃基) R—OH+R′—OH
R—OH+R′—OH R—O—R′+H2O (R、R′ 表示烃基)
R—O—R′+H2O (R、R′ 表示烃基)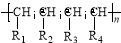

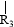
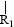 nCH=CH+nCH=CH
nCH=CH+nCH=CH (R1~R4表示氢或烃基)
(R1~R4表示氢或烃基)