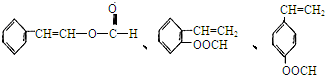题目内容
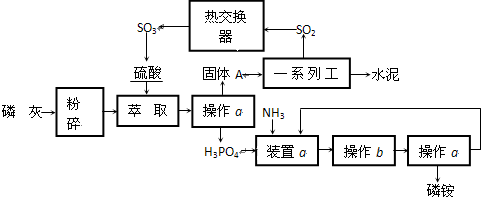
Ⅰ.物质的分离和提纯有多种方法.物质分离、提纯方案的设计在科学研究和工业生产中占有十分重要的地位.工业上冶炼铝的原料是铝土矿(主要成分是Al2O3,杂质为Fe2O3、SiO2等,已知SiO2是不溶于水的酸性氧化物,Fe2O3是不溶于水的碱性氧化物).某研究小组设计的提纯Al2O3的方案如下:

(1)写出沉淀A的化学式: .
(2)加入过量的NaOH溶液,过滤后的滤液中含有的溶质有 .
(3)写出由沉淀A-→Al2O3的化学方程式: ,通入过量CO2生成沉淀A时反应的离子方程式为 .
Ⅱ.按照要求回答下列问题:
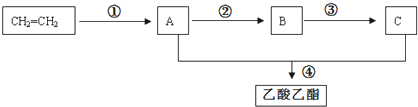
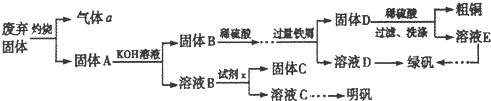
A、B、C、D、E是常见化合物或单质,有如下转化关系 (略去条件和副产品).
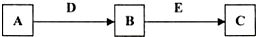
(1)若A为黄绿色气体单质,D、E为生活中常见的两种金属,其中E是一种红色光亮的物质.
①写出向B的溶液中加入足量D的离子反应方程式 .
②向①所得的溶液中加入NaOH溶液,并在空气中放置的现象是: ,写出固体在空气中放置的化学反应方程式: .

(1)写出沉淀A的化学式:
(2)加入过量的NaOH溶液,过滤后的滤液中含有的溶质有
(3)写出由沉淀A-→Al2O3的化学方程式:
Ⅱ.按照要求回答下列问题:
A、B、C、D、E是常见化合物或单质,有如下转化关系 (略去条件和副产品).

(1)若A为黄绿色气体单质,D、E为生活中常见的两种金属,其中E是一种红色光亮的物质.
①写出向B的溶液中加入足量D的离子反应方程式
②向①所得的溶液中加入NaOH溶液,并在空气中放置的现象是:
考点:物质分离和提纯的方法和基本操作综合应用,无机物的推断
专题:推断题,实验设计题
分析:Ⅰ、铝土矿(主要成分是Al2O3,杂质为Fe2O3、SiO2等,已知SiO2是不溶于水的酸性氧化物,Fe2O3是不溶于水的碱性氧化物),加入盐酸溶解过滤,固体为二氧化硅,滤液1为氯化铝、氯化铁溶液,滤液中加入过量氢氧化钠溶液过滤得到沉淀为氢氧化铁,滤液2为偏铝酸钠溶液,通入过量二氧化碳反应生成氢氧化铝沉淀和碳酸氢钠,氢氧化铝加热分解生成氧化铝;
(1)沉淀A为氢氧化铝;
(2)加入过量的NaOH溶液,反应生成偏氯酸钠溶液,氯化钠溶液;
(3)由沉淀A-→Al2O3的化学方程式为氢氧化铝加热分解生成;通入过量CO2生成沉淀A时反应生成氢氧化铝沉淀和碳酸氢钠溶液;
Ⅱ、(1)①若A为黄绿色气体单质为Cl2,D、E为生活中常见的两种金属,其中E是一种红色光亮的物质为Cu,D为Fe;Cl2
FeCl3
FeCl2;
②向①所得的溶液中加入NaOH溶液,反应生成氢氧化亚铁,空气中被氧气氧化白色转化为灰绿色,最后变化为红褐色沉淀氢氧化铁.
(1)沉淀A为氢氧化铝;
(2)加入过量的NaOH溶液,反应生成偏氯酸钠溶液,氯化钠溶液;
(3)由沉淀A-→Al2O3的化学方程式为氢氧化铝加热分解生成;通入过量CO2生成沉淀A时反应生成氢氧化铝沉淀和碳酸氢钠溶液;
Ⅱ、(1)①若A为黄绿色气体单质为Cl2,D、E为生活中常见的两种金属,其中E是一种红色光亮的物质为Cu,D为Fe;Cl2
| Fe |
| Cu |
②向①所得的溶液中加入NaOH溶液,反应生成氢氧化亚铁,空气中被氧气氧化白色转化为灰绿色,最后变化为红褐色沉淀氢氧化铁.
解答:
解:Ⅰ、铝土矿(主要成分是Al2O3,杂质为Fe2O3、SiO2等,已知SiO2是不溶于水的酸性氧化物,Fe2O3是不溶于水的碱性氧化物),加入盐酸溶解过滤,固体为二氧化硅,滤液1为氯化铝、氯化铁溶液,滤液中加入过量氢氧化钠溶液过滤得到沉淀为氢氧化铁,滤液2为偏铝酸钠溶液,通入过量二氧化碳反应生成氢氧化铝沉淀和碳酸氢钠,氢氧化铝加热分解生成氧化铝;
(1)沉淀A为氢氧化铝,沉淀A的化学式为Al(OH)3,故答案为:Al(OH)3;
(2)加入过量的NaOH溶液,反应生成偏氯酸钠溶液,氯化钠溶液,过滤后的滤液中含有的溶质有NaOH、NaAlO2、NaCl,故答案为:NaOH、NaAlO2、NaCl;
(3)由沉淀A-→Al2O3的化学方程式为氢氧化铝加热分解生成,反应的化学方程式为:2Al(OH)3
Al2O3+3H2O;通入过量CO2生成沉淀A时反应生成氢氧化铝沉淀和碳酸氢钠溶液,反应的离子方程式为:AlO2-+CO2+2H2O═Al(OH)3↓+HCO3-;
故答案为:2Al(OH)3
Al2O3+3H2O;AlO2-+CO2+2H2O═Al(OH)3↓+HCO3-;
Ⅱ、(1)①若A为黄绿色气体单质为Cl2,D、E为生活中常见的两种金属,其中E是一种红色光亮的物质为Cu,D为Fe,转化为Cl2
FeCl3
FeCl2,向B的溶液中加入足量D的离子反应方程式为Fe+2Fe3+=3Fe2+,
故答案为:Fe+2Fe3+=3Fe2+;
②向①所得的溶液中加入NaOH溶液,反应生成氢氧化亚铁,空气中被氧气氧化白色转化为灰绿色,最后变化为红褐色沉淀氢氧化铁,反应为4Fe(OH)2+O2+2H2O=4Fe(OH)3,
故答案为:生成白色絮状沉淀迅速变成灰绿色,最后变成红褐色,4Fe(OH)2+O2+2H2O=4Fe(OH)3.
(1)沉淀A为氢氧化铝,沉淀A的化学式为Al(OH)3,故答案为:Al(OH)3;
(2)加入过量的NaOH溶液,反应生成偏氯酸钠溶液,氯化钠溶液,过滤后的滤液中含有的溶质有NaOH、NaAlO2、NaCl,故答案为:NaOH、NaAlO2、NaCl;
(3)由沉淀A-→Al2O3的化学方程式为氢氧化铝加热分解生成,反应的化学方程式为:2Al(OH)3
| ||
故答案为:2Al(OH)3
| ||
Ⅱ、(1)①若A为黄绿色气体单质为Cl2,D、E为生活中常见的两种金属,其中E是一种红色光亮的物质为Cu,D为Fe,转化为Cl2
| Fe |
| Cu |
故答案为:Fe+2Fe3+=3Fe2+;
②向①所得的溶液中加入NaOH溶液,反应生成氢氧化亚铁,空气中被氧气氧化白色转化为灰绿色,最后变化为红褐色沉淀氢氧化铁,反应为4Fe(OH)2+O2+2H2O=4Fe(OH)3,
故答案为:生成白色絮状沉淀迅速变成灰绿色,最后变成红褐色,4Fe(OH)2+O2+2H2O=4Fe(OH)3.
点评:本题考查了物质分离提纯的分析判断,物质性质的理解应用,掌握基础是关键,题目难度中等.

练习册系列答案
相关题目
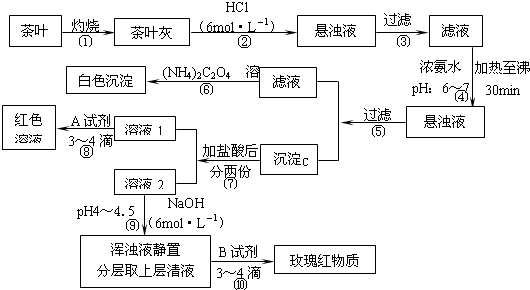
反应①是自海藻灰中提取碘的主要反应,反应②是自智利硝石中提取碘的主要反应:①2NaI+MnO2+3H2SO4=2NaHSO4+MnSO4+2H2O+I2;②2NaIO3+5NaHSO3=2Na2SO4+3NaHSO4+H2O+I2.已知NaIO3的氧化性与MnO2相近,下列有关说法正确的是( )
| A、两个反应中生成等量的I2时转移的电子数相等 |
| B、I2在反应①②中都是氧化产物 |
| C、NaI和NaIO3在一定条件下能反应生成I2 |
| D、NaIO3在任何化学反应中只能作氧化剂,不能作还原剂 |
分子式为C5H10O2属于羧酸的同分异构体数目有( )
| A、3种 | B、4种 | C、5种 | D、6种 |
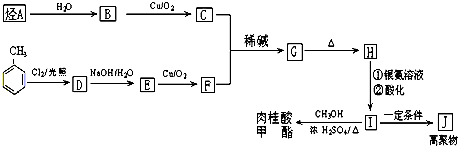
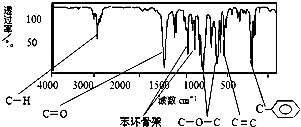 肉桂酸甲酯是调制具有草莓、葡萄、樱桃、香子兰等香味的食用香精,用于肥皂、洗涤剂、风味剂和糕点的调味,在医药工业中作为有机合成的中间体.
肉桂酸甲酯是调制具有草莓、葡萄、樱桃、香子兰等香味的食用香精,用于肥皂、洗涤剂、风味剂和糕点的调味,在医药工业中作为有机合成的中间体.