题目内容
对工业废水和生活污水进行处理是防止水体污染的主要措施.
(1)水的净化和软化的区别是
(2)①在实验室中过滤操作需要用到的玻璃仪器有 .
②下列试剂能够用来对自来水进行杀菌消毒,且不会造成二次污染的是 (填字母).
a.福尔马林 b.漂白粉 c.臭氧 d.氯气
(3)Na2FeO4是一种新型水处理剂,工业上可用FeSO4制备Na2FeO4其工艺流程如图:

①工业上常用硫酸亚铁作混凝剂除去天然水中含有的悬浮物和胶体,为了达到更好的效果,要将待处理水的pH调到9左右,再加入绿矾.请解释这一做法的原因 (用必要的离子方程式和文字描述).
②假设每步反应均是完全的,若制取3mol NaZFe04,需要NaClO固体 g.
③写出第一步在酸性环境下加入H202的离子反应方程式 .
(4)石灰纯碱法是常用的硬水软化方法,已知25℃时Ksp(CaCO3)=2.8×10-9,现将等体积的Ca(OH)2溶液与Na2CO3溶液混合(假设溶液体积具有加和性),若Na2CO3溶液的浓度为5.6×10-5mol?L-1,则生成沉淀所需Ca(0H)2溶液的最小浓度为 .
(1)水的净化和软化的区别是
(2)①在实验室中过滤操作需要用到的玻璃仪器有
②下列试剂能够用来对自来水进行杀菌消毒,且不会造成二次污染的是
a.福尔马林 b.漂白粉 c.臭氧 d.氯气
(3)Na2FeO4是一种新型水处理剂,工业上可用FeSO4制备Na2FeO4其工艺流程如图:

①工业上常用硫酸亚铁作混凝剂除去天然水中含有的悬浮物和胶体,为了达到更好的效果,要将待处理水的pH调到9左右,再加入绿矾.请解释这一做法的原因
②假设每步反应均是完全的,若制取3mol NaZFe04,需要NaClO固体
③写出第一步在酸性环境下加入H202的离子反应方程式
(4)石灰纯碱法是常用的硬水软化方法,已知25℃时Ksp(CaCO3)=2.8×10-9,现将等体积的Ca(OH)2溶液与Na2CO3溶液混合(假设溶液体积具有加和性),若Na2CO3溶液的浓度为5.6×10-5mol?L-1,则生成沉淀所需Ca(0H)2溶液的最小浓度为
考点:"三废"处理与环境保护
专题:化学应用
分析:(1)根据水的净化和软化的本质来分析;
(2)①过滤除去溶液中的不溶性杂质的方法,根据过滤装置来分析;
②对自来水进行杀菌消毒,且不会造成二次污染,只有臭氧的还原产物对水无污染;
(3)①将待处理水的pH调到9左右,再加入绿矾,可得到铁离子,水解生成胶体;
②发生氧化还原反应生成Na2FeO4;
③H202在酸性条件下能将Fe2+氧化为Fe3+,H202被还原为水,据此写出离子方程式;
(4)Na2CO3溶液的浓度为2.8×10-5mol/L,等体积混合后溶液中c(CO32-)=1.4×10-5mol/L,根据Ksp=c(CO32-)?c(Ca2+)计算沉淀时混合溶液中c(Ca2+),以此来解答.
(2)①过滤除去溶液中的不溶性杂质的方法,根据过滤装置来分析;
②对自来水进行杀菌消毒,且不会造成二次污染,只有臭氧的还原产物对水无污染;
(3)①将待处理水的pH调到9左右,再加入绿矾,可得到铁离子,水解生成胶体;
②发生氧化还原反应生成Na2FeO4;
③H202在酸性条件下能将Fe2+氧化为Fe3+,H202被还原为水,据此写出离子方程式;
(4)Na2CO3溶液的浓度为2.8×10-5mol/L,等体积混合后溶液中c(CO32-)=1.4×10-5mol/L,根据Ksp=c(CO32-)?c(Ca2+)计算沉淀时混合溶液中c(Ca2+),以此来解答.
解答:
解:(1)水的净化即水的除杂,除去水中的杂质;水的软化是将硬水转化为软水,降低钙离子和镁离子,
故答案为:水的净化是除去悬浮物和污染物,而水的软化是除去水中较多的钙离子和镁离子;
(2)①过滤除去溶液中的不溶性杂质的方法,使用的玻璃仪器有玻璃棒、烧杯、普通漏斗(胶头滴管),故答案为:玻璃棒、烧杯、普通漏斗(胶头滴管);
②福尔马林有毒,含氯物质可导致二次污染,则能够用来对自来水进行杀菌消毒,且不会造成二次污染的只有臭氧,故答案为:c;
(3)①工业上常用硫酸亚铁作混凝剂除去天然水中含有的悬浮物和胶体,为了达到更好的效果,要将待处理水的pH调到9左右,再加绿矾,原因:Fe2+在碱性条件下易被氧化成Fe3+,进而水解生成Fe(OH)3胶体,起到较好的混凝作用,4Fe2++O2+2H2O+8OH-=4Fe(OH)3(胶体),
故答案为:Fe2+在碱性条件下易被氧化成Fe3+,进而水解生成Fe(OH)3胶体,起到较好的混凝作用,4Fe2++O2+2H2O+8OH-═4Fe(OH)3(胶体);
②由Fe(0H)3制取Na2FeO4的化学方程式为:2Fe(OH)3+3NaClO+4NaOH═2Na2FeO4+3NaCl+5H2O,设需要的NaClO的物质的量为Xmol,
3 2
Xmol 3mol
可得:
=
解得X=4.5mol
则NaClO的质量m=nM=4.5mol×74.5g/mol=335.25g
故答案为:335.25;
③H202在酸性条件下能将Fe2+氧化为Fe3+,H202被还原为水,故离子方程式为:2Fe2++H2O2+2H+=2Fe3++2H2O,
故答案为:2Fe2++H2O2+2H+=2Fe3++2H2O;
(4)Na2CO3溶液的浓度为5.6×10-5mol/L,等体积混合后溶液中c(CO32-)=
×5.6×10-5mol/L=2.8×10-5mol/L,根据Ksp=c(CO32-)?c(Ca2+)=2.8×10-9可知,c(Ca2+)=
mol/L=1×10-4mol/L,原溶液Ca(OH)2溶液的最小浓度为混合溶液中c(Ca2+)的2倍,故原溶液Ca(OH)2溶液的最小浓度为2×1×10-4mol/L=2×10-4mol/L,故答案为:2×10-4mol/L.
故答案为:水的净化是除去悬浮物和污染物,而水的软化是除去水中较多的钙离子和镁离子;
(2)①过滤除去溶液中的不溶性杂质的方法,使用的玻璃仪器有玻璃棒、烧杯、普通漏斗(胶头滴管),故答案为:玻璃棒、烧杯、普通漏斗(胶头滴管);
②福尔马林有毒,含氯物质可导致二次污染,则能够用来对自来水进行杀菌消毒,且不会造成二次污染的只有臭氧,故答案为:c;
(3)①工业上常用硫酸亚铁作混凝剂除去天然水中含有的悬浮物和胶体,为了达到更好的效果,要将待处理水的pH调到9左右,再加绿矾,原因:Fe2+在碱性条件下易被氧化成Fe3+,进而水解生成Fe(OH)3胶体,起到较好的混凝作用,4Fe2++O2+2H2O+8OH-=4Fe(OH)3(胶体),
故答案为:Fe2+在碱性条件下易被氧化成Fe3+,进而水解生成Fe(OH)3胶体,起到较好的混凝作用,4Fe2++O2+2H2O+8OH-═4Fe(OH)3(胶体);
②由Fe(0H)3制取Na2FeO4的化学方程式为:2Fe(OH)3+3NaClO+4NaOH═2Na2FeO4+3NaCl+5H2O,设需要的NaClO的物质的量为Xmol,
3 2
Xmol 3mol
可得:
| 3 |
| X |
| 2 |
| 3 |
解得X=4.5mol
则NaClO的质量m=nM=4.5mol×74.5g/mol=335.25g
故答案为:335.25;
③H202在酸性条件下能将Fe2+氧化为Fe3+,H202被还原为水,故离子方程式为:2Fe2++H2O2+2H+=2Fe3++2H2O,
故答案为:2Fe2++H2O2+2H+=2Fe3++2H2O;
(4)Na2CO3溶液的浓度为5.6×10-5mol/L,等体积混合后溶液中c(CO32-)=
| 1 |
| 2 |
| 2.8×10-9 |
| 2.8×10-5 |
点评:本题考查较综合,涉及混合物分离提纯、溶度积的计算、氧化还原反应及应用等,注重高频考点的考查,综合性较强,题目难度较大,注意化学与生活的联系.

练习册系列答案
 芒果教辅达标测试卷系列答案
芒果教辅达标测试卷系列答案
相关题目
下列相关实验的现象或结论正确的是( )
| A、向NaAlO2溶液中滴入NaHCO3溶液有白色沉淀,则AlO2-结合质子能力比CO32-强 |
| B、向少量的稀溴水中滴入饱和苯酚溶液立即产生白色沉淀 |
| C、检验废铁屑溶于盐酸后所得的溶液中是否含有Fe2+,可向其中加入酸性KMnO4溶液,根据其是否褪色进行判断 |
| D、加入硫酸铜可使锌与稀硫酸的反应速率加快,说明Cu2+具有催化作用 |
用下列实验装置进行相应实验,设计正确且能达到实验目的是( )
A、 用装置制取少量H2: |
B、 用装置分离Na2CO3溶液和CH3COOC2H5的混合物 |
C、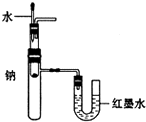 用装置验证Na和水反应的热效应 |
D、 用装置蒸干A1Cl3溶液制备无水AlC13 |
下列解释不科学的是( )
| A、“水滴石穿”是溶解了CO2的雨水与CaCO3长期作用生成了可溶解的Ca(HCO3)2的缘故 |
| B、地沟油由于混有一些对人体有害的杂质而不能食用,可加工制成和从石油中提取的柴油成分完全相同的生物柴油 |
| C、长期盛放NaOH溶液的滴瓶不易打开,主要是由于NaOH能与玻璃中的SiO2反应生成硅酸钠导致瓶塞粘住的缘故 |
| D、黄铜(铜锌合金)不易产生铜绿,这是因为发生电化学腐蚀时,锌被腐蚀而保护了铜 |

 +R′-Cl→
+R′-Cl→ +HCl
+HCl


 (1)已知下列反应:
(1)已知下列反应:
