题目内容
X、Y、Z、W、Q五种元素原子序数依次增大,X为地壳中含量最高的元素,在周期表中Y与X、Z、Q相邻,Q与X最高能层上的电子数相同,W原子核外有七种不同能级的电子,且最高能级上没有未成对电子,W与X可形成W2X和WX两种化合物。
回答下列问题:
(1)X能与原子序数最小的元素形成原子个数比为1:1的分子,该分子的电子式为 。
(2)W2+的核外电子排布式为 。
(3)Z单质能溶于水,水液呈 色,在其中通人Y的某种氧化物,溶液颜色褪去,用化学方程式表示原因 。
(4)Y、Z元素的第一电离能Y Z(填“>”、“<”或“=”)。 X与地壳中含量第二的元素形成的化合物所属的晶体类型为 。
(5)已知X分别与元素碳、氮形成化合物有如下反应:
2CX(g)+X2(g)=2CX2(g) △H=—566.0kJ·mol-1
N2(g)+X2(g)=2NX(g) △H=189.5kJ·mol-1
2NX(g)+X2(g)=2NX2(g) △H=—112.97kJ·mol-1
写出NX2与CX反应生成大气中存在的两种气态物质的热化学方程式: 。
(6)Y与磷原子形成P4Y3分子,该分子中没有π键,且各原子最外层均已达8电子结构,则一个P4Y3分子中含有的极性键和非极性键的个数分别为 个、 个。
(15分)
(1)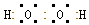 (2分)
(2分)
(2)1s22s22p63s23p63d9 (2分)
(3)黄绿 (1分) Cl2+SO2+2H2O=2HCl+H2SO4(2分)
(4)< (1分)原子晶体(1分)
(5)NO2(g)+4CO(g)= N2(g)+4CO2(g) ΔH =-1208.53 kJ·mol-1 (3分)
(6)6 (2分) 3 (2分)
【解析】
试题分析:地壳中含量最多的为氧,而X、Q同主族,Y和X、Z、Q均相邻,故X、Y、Q同族,且Y在中间,则Y为硫,Q为硒,又Y、Z相邻,且Z的原子序数大于Y,故Z为氯,W有7个能级,分别为1s、2s、2p、3s、3p、3d、4s,且最高能级没有未成对电子,则3d能级上有10个电子,根据其形成的两种氧化物确定其为铜。
(1)O能与原子序数最小的元素H形成原子个数比为1:1的分子H2O2。
(2)Cu2+的核外电子排布式为1s22s22p63s23p63d9。
(3)Z的单质为氯气,水溶液呈黄绿色;在氯水中通人SO2,发生氧化还原反应,溶液颜色褪去。
(4)同一周期从左至右电离能逐渐升高,故S<Cl;SiO2为典型的原子晶体。
(5)根据盖斯定律可以计算得到反应热,写出热化学方程式。
(6)可以想象为在P4(正四面体结构)分子中的每个P-P键中放入一个S原子,故有6个极性键、3个非极性键。
考点:本题以元素推断为基础,考查原子结构、分子结构、元素周期律、元素及化合物、热化学方程式的书写、盖斯定律等知识。