题目内容
14.事实证明,能设计成原电池的反应通常是放热反应,下列化学反应在理论上可以设计成原电池的是 ( )| A. | C(s)+H2O(g)=CO(g)+H2(g)△H>0 | B. | NaOH(aq)+HC1(aq)=NaC1(aq)+H2O(1)△H<0 | ||
| C. | 2CO(g)+O2(g)=2CO2(1)△H<0 | D. | 2H2(g)+O2(g)═2H2O(l)△H<0 |
分析 常温下属于氧化还原反应的放热反应,可设计为原电池,存在元素化合价变化的反应为氧化还原反应,以此解答该题.
解答 解:A.C(s)+CO2(g)=2CO(g)△H>0,为氧化还原反应,但为吸热反应,不能设计为原电池,故A错误;
B.NaOH(aq)+HC1(aq)=NaC1(aq)+H2O(1)△H<0,不属于氧化还原反应,不能设计为原电池,故B错误;
C.2CO(g)+O2(g)=2CO2(1)△H<0,为氧化还原反应,为放热反应,能设计为原电池,故C正确;
D.2H2(g)+O2(g)═2H2O(l)△H<0,为氧化还原反应,为放热反应,能设计为原电池,故D正确.
故选CD.
点评 本题考查原电池的设计,为高频考点,侧重于学生的分析能力的考查,明确原电池与氧化还原反应的关系及负极发生氧化反应是解答本题的关键,题目难度不大.

练习册系列答案
 举一反三期末百分冲刺卷系列答案
举一反三期末百分冲刺卷系列答案
相关题目
5.下列说法中正确的是( )
| A. | 明矾的化学式为Al2(SO4)3•12H2O | |
| B. | 明矾溶于水产生Al(OH)3胶体:Al3++3H2O═Al(OH)3↓+3H+ | |
| C. | AlCl3溶液与浓氨水反应有白色沉淀生成 | |
| D. | Al是重要的金属元素,其对应的氧化物为碱性氧化物 |
9.化学无处不在,与化学有关的说法不正确的是( )
| A. | 绚丽缤纷的烟花中可能添加了含钾、钠、钙、铜等某些金属元素的物质 | |
| B. | 回收废弃塑料制成燃油替代汽油、柴油,可减轻环境污染和节约化石能源 | |
| C. | 为防止电池中的重金属等污染土壤和水体,应积极开友废电池的综合利用技术 | |
| D. | 生铁炼钢时必须完全除去生铁中的碳,以避免因钢铁中含有碳而发生电化学腐蚀 |
19.某溶液中只可能含有下列离子中的几种:K+、NO3-、SO42-、NH4+、CO32-(不考虑溶液中少量的H+和OH-),取200mL该溶液,分为两等份进行下列实验:
实验1:第一份加入足量的烧碱并加热,产生的气体在标准状况下为224mL;
实验2:第二份先加入足量的盐酸,无现象,再加入足量的BaCl2溶液,得固体2.33g.
下列说法正确的是( )
实验1:第一份加入足量的烧碱并加热,产生的气体在标准状况下为224mL;
实验2:第二份先加入足量的盐酸,无现象,再加入足量的BaCl2溶液,得固体2.33g.
下列说法正确的是( )
| A. | 该溶液中可能含K+ | |
| B. | 该溶液中肯定含有NO3-、SO42-、NH4+、CO32- | |
| C. | 该溶液中一定不含NO3- | |
| D. | 该溶液中一定含K+,且c(K+)≥0.1mol/L |
3.对于反应A2+3B2=2C来说,以下表示中,化学反应速率最快的是( )
| A. | v(B2)=0.8 mol/(L•s) | B. | v(A2)=0.3 mol/(L•s) | C. | v(C)=0.8 mol/(L•s) | D. | v(B2)=0.9 mol/(L•s) |
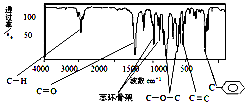
 (不考虑立体异构)
(不考虑立体异构)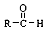 +CH3CHO$\stackrel{稀碱}{→}$
+CH3CHO$\stackrel{稀碱}{→}$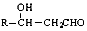 $\stackrel{-H_{2}O}{→}$RCH=CHCHO
$\stackrel{-H_{2}O}{→}$RCH=CHCHO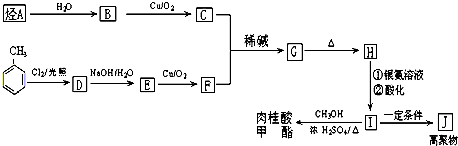

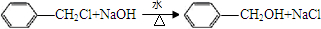
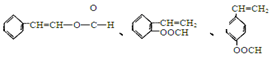
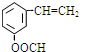 、
、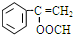 .
.