题目内容
下列离子方程式中正确的是( )
| A、用FeCl3溶液腐蚀印刷电路板:Fe3++Cu=Fe2++Cu2+ | ||
B、等体积、等物质的量浓度的NaHCO3溶液和Ca(OH)2溶液混合:
| ||
| C、向稀硫酸中加入铜粉:Cu+2H+=Cu2++H2↑ | ||
| D、向AlCl3溶液中加入过量氨水:Al3++3OH-=Al(OH)3↓ |
考点:离子方程式的书写
专题:离子反应专题
分析:A.电荷不守恒,得失电子不守恒;
B.NaHCO3溶液和Ca(OH)2溶液1:1反应生成碳酸钙、氢氧化钠和水;
C.不符合反应的客观事实,铜与稀硫酸不反应;
D.一水合氨为弱电解质,应保留化学式.
B.NaHCO3溶液和Ca(OH)2溶液1:1反应生成碳酸钙、氢氧化钠和水;
C.不符合反应的客观事实,铜与稀硫酸不反应;
D.一水合氨为弱电解质,应保留化学式.
解答:
解:A.用FeCl3溶液腐蚀印刷电路板,离子方程式:2Fe3++Cu=2Fe2++Cu2+,故A错误;
B.等体积、等物质的量浓度的NaHCO3溶液和Ca(OH)2溶液混合,离子方程式为:HCO3-+Ca2++OH-=CaCO3↓+H2O,故B正确;
C.向稀硫酸中加入铜粉不发生反应;
D.向AlCl3溶液中加入过量氨水,离子方程式:Al3++3NH3?H2O=Al(OH)3↓+3NH4+,故D错误;
故选:B.
B.等体积、等物质的量浓度的NaHCO3溶液和Ca(OH)2溶液混合,离子方程式为:HCO3-+Ca2++OH-=CaCO3↓+H2O,故B正确;
C.向稀硫酸中加入铜粉不发生反应;
D.向AlCl3溶液中加入过量氨水,离子方程式:Al3++3NH3?H2O=Al(OH)3↓+3NH4+,故D错误;
故选:B.
点评:本题考查了离子方程式的书写,书写离子方程式时应注意必须符合反应的客观事实、必须遵循电荷守恒、原子个数守恒,题目难度不大.

练习册系列答案
相关题目
湿润的淀粉碘化钾试纸遇臭氧变蓝,化学方程式为:2KI+O3+H2O=2KOH+I2+O2下列叙述正确的是( )
| A、O3在反应中被还原为O2 |
| B、该反应的还原剂是H2O |
| C、1molO3在反应中得到2mol电子 |
| D、反应中氧化剂与还原剂的物质的量之比为2:1 |
下列各组在溶液中反应,不管反应物的量是多少,都能用同一离子方程式表示的是( )
| A、FeI2与Cl2 |
| B、FeCl3与H2S |
| C、HCl与Na2CO3 |
| D、NaHCO3与Ca(OH)2 |
下列有关化学电池的说法中正确的是( )
| A、化学电池只能将化学能转化为电能 |
| B、燃料电池能将全部化学能转化为电能 |
| C、锌银电池比能量大,电压稳定,储存时间长 |
| D、一次电池包括干电池和蓄电池 |
化学科学需要借助化学专用语言描述,下列有关化学用语正确的是( )
A、CO2的球棍模型示意图: | ||
B、Cl-的结构示意图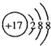 | ||
C、质量数为37的氯原子
| ||
| D、N2的结构式::N≡N: |
位于元素周期表第三周期ⅦA族的元素是( )
| A、Li | B、O | C、Al | D、Cl |
丙烯醛的结构是CH2=CH-CHO,下列关于它的性质的叙述中,错误的是( )
| A、能使溴水和高锰酸钾溶液褪色 |
| B、能被新制的氢氧化铜悬浊液氧化 |
| C、在一定条件下,与氢气充分反应生成丙醇 |
| D、能发生银镜反应,体现氧化性 |
下列各种高聚物中,具有热固性的是( )
| A、有机玻璃 | B、聚氯乙烯 |
| C、聚丙烯 | D、酚醛塑料 |



 A.核磁共振氢谱 B.红外光谱C.质谱
A.核磁共振氢谱 B.红外光谱C.质谱