题目内容
已知酸性溶液中还原性的顺序为SO32﹣>I﹣>Fe2+>Br﹣>Cl﹣,下列反应不能发生的是( )
A.2 Fe3++SO32﹣+H2O→2Fe2++SO42﹣+2H+
Fe3++SO32﹣+H2O→2Fe2++SO42﹣+2H+
B.I2+SO32﹣+H2O→SO42﹣+2I﹣+2H+
C.2Fe2++I2→2Fe3++2I﹣
D.Br2+SO32﹣+H2O→SO42﹣+2Br﹣+2H+
练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
3.镁、铝、铁三种金属分别与足量的盐酸反应,生成相同质量的氢气,则参加反应的三种金属( )
| A. | 物质的量相等 | B. | 失去电子的物质的量相等 | ||
| C. | 质量比为24:27:26 | D. | 质量比为12:18:28 |
18.下列各盐中可以用“酸性氧化物+碱制得的是( )
| A. | FeCl3 | B. | Na2S | C. | NH4Cl | D. | CaCO3 |
若用12 mol•L-1的浓盐酸配制0.10 mol•L-1的稀盐酸480 mL,回答下列问题:
(1)量取浓盐酸的体积为 mL,如果实验室有5mL、10mL、50mL量筒,应选用 mL量筒最好。若量取时发现量筒不干净,用水洗净后直接量取,所配溶液浓度将 (偏高、偏低、无影响)。
(2)配制时应选用的容量瓶规格为 mL 。
(3)配制时所需仪器除了容量瓶和量筒外,还需要的仪器有: 。
(4) 配制时,将量取的浓盐酸沿烧杯内壁慢慢注入约100mL水里,并不断搅拌,目的是 。
(5)若实验遇下列情况,所配溶液的浓度会有什么影响(填“偏高”,“偏低”或“无影响”)
A.溶解后没有冷却便进行定容________________ |
B.最后定容时,俯视观察液面与容量瓶刻度线________________ |
C.容量瓶内壁附有水珠而未干燥处理_______________ |
D.用量筒量取所需浓盐酸体积时俯视观察 。 |
3.下列比较中正确的是( )
| A. | 碱性:KOH>Mg(OH)2>NaOH | B. | 酸性:H3PO4>H2SO4>HClO4 | ||
| C. | 原子半径:K>Na>Mg | D. | 氢化物稳定性:NH3>H2O>HF |


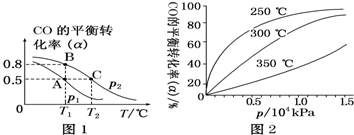 煤的气化可以减少环境污染,而且生成的CO和H2被称作合成气,能合成很多基础有机化工原料.
煤的气化可以减少环境污染,而且生成的CO和H2被称作合成气,能合成很多基础有机化工原料.