题目内容
14.下列叙述正确的是( )| A. | 甲酸溶液导电性比乙酸溶液导电性强,说明乙酸是弱酸 | |
| B. | 硫酸钾溶于水能导电,所以硫酸钾是电解质 | |
| C. | 强电解质一定是含有离子键,弱电解质中一定含弱极性共价键 | |
| D. | 固态磷酸是电解质,所以磷酸在熔融状态下和水溶液中都能导电 |
分析 A.不能根据溶液的导电性判断酸性的强弱;
B.在水溶液中或熔融状态下能导电的化合物是电解质;
C.强电解质不一定含有离子键,如HCl;
D.当物质存在自由移动的离子或电子时,可导电.
解答 解:A.在溶液中部分电离的酸是弱酸,不能根据溶液的导电性判断酸性的强弱,故A错误;
B.在水溶液中或熔融状态下能导电的化合物是电解质,硫酸钾溶于水能导电,所以硫酸钾是电解质,故B正确;
C.强电解质不一定含有离子键,如HCl,如弱电解质中也可能存在强极性键,如HF,故C错误;
D.导电的条件是物质存在自由移动的离子或电子,磷酸在熔融状态时不能电离,所以不导电,故D错误.
故选B.
点评 本题考查较为综合,涉及电解质的电离、电解质的强弱以及化学键的类型等知识,为高考常见题型,侧重于学生的分析能力和基础知识的综合理解和运用的考查,难度不大,注意相关基础知识的积累.

练习册系列答案
相关题目
4.下列有关物质的性质与用途具有对应关系的是( )
| A. | NH3极易溶于水,可用于工业制冷剂 | |
| B. | HNO3具有酸性,可用于制备硝酸盐原料 | |
| C. | NH4 NO3易溶于水,可用于制造高温材料 | |
| D. | N2难溶于水,可用于合成氨原料 |
5.已知W、X、Y、Z为原子序数依次增大的短周期元素,W、Z同主族,X、Y、Z同周期,下列说法正确的是( )
| A. | W、X、Y、Z不可能全为非金属元素 | |
| B. | W的简单气态氢化物的沸点一定高于Z的简单气态氢化物的沸点 | |
| C. | 若W、X、Y的原子序数依次相差2,则在工业上制备Y的单质时,W、X、Y形成的化合物起到了重要作用 | |
| D. | 若W与X的原子序数相差4,则Z与X形成的化合物一定是离子化合物 |
2.下列电子式的书写正确的是( )
| A. | Mg2+ | B. | S2- | C. | 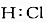 | D. | 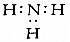 |
9.复印机工作时,空气中的氧气可以转化为臭氧:3O2═2O3,下列有关说法正确的是( )
| A. | 该变化属于物理变化 | B. | 1mol 臭氧比 1mol 氧气的能量高 | ||
| C. | 空气中臭氧比氧气更稳定 | D. | 氧分子中的化学键断裂会放出能量 |
19.下列物质的熔、沸点高低顺序中,正确的是( )
| A. | 金刚石>晶体硅>二氧化硅>碳化硅 | B. | I2>Br2>Cl2>F2 | ||
| C. | H2Te>H2Se>H2S>H2O | D. | 金刚石>CsCl>NaCl>钠 |
6.下列反应离子方程式正确的是( )
| A. | 向NaOH溶液中通入氯气:2OH-+Cl2═Cl-+ClO-+H2O | |
| B. | 氨气与盐酸反应:NH3+HCl═NH4++Cl- | |
| C. | 碳酸钙跟醋酸反应:CaCO3+2H+═Ca2++CO2↑+H2O | |
| D. | 将稀硝酸滴在铁片上:Fe+2H+═Fe2++H2↑ |
3.X、Y、Z、M为原子序数依次增大的四种短周期元素.X、Y、Z同周期且相邻,M为唯一一种金属元素且最外层电子数为X、Y、Z最外层电子数之和的$\frac{1}{5}$.下列说法不正确的是( )
| A. | X、Y、Z形成的气态氢化物中稳定性最强的是H2Z | |
| B. | Y所在族的氢化物的沸点最高的是Y对应的氢化物 | |
| C. | 离子半径的大小:M>Y>Z | |
| D. | M的最高价氧化物对应的水化物可以溶解于Y对应最高价含氧酸 |