题目内容
氯化硼的熔点为-107℃,沸点为12.5℃,在其分子中键与键之间的夹角为120°,它能水解,有关叙述正确的是( )
①氯化硼液态时能导电而固态时不导电 ②氯化硼中心原子采用sp杂化
③氯化硼分子呈正三角形,属非极性分子 ④其分子空间结构类似CH2O.
①氯化硼液态时能导电而固态时不导电 ②氯化硼中心原子采用sp杂化
③氯化硼分子呈正三角形,属非极性分子 ④其分子空间结构类似CH2O.
| A、①④ | B、②③ | C、③④ | D、①③ |
考点:不同晶体的结构微粒及微粒间作用力的区别,判断简单分子或离子的构型,原子轨道杂化方式及杂化类型判断
专题:化学键与晶体结构
分析:①氯化硼是共价化合物;
②三氯化硼中的硼为sp2杂化;
③三氯化硼中的硼为sp2杂化,无孤对电子;
④三氯化硼是平面三角形结构.
②三氯化硼中的硼为sp2杂化;
③三氯化硼中的硼为sp2杂化,无孤对电子;
④三氯化硼是平面三角形结构.
解答:
解:①氯化硼是共价化合物液态时不能电离出自由移动的离子,所以不能导电,故错误;
②三氯化硼中的硼的成键电子对为3,孤电子对数=
(3-3×1)=0,则价层电子对数为3,为sp2杂化,故错误;
③三氯化硼中的硼为sp2杂化,无孤对电子,分子中键与键之间的夹角为120°,是平面三角形结构,空间结构对称属于非极性分子,故正确;
④三氯化硼是平面三角形结构,CH2O的分子结构为平面三角形,则二者分子空间结构类似,故正确.
故选C.
②三氯化硼中的硼的成键电子对为3,孤电子对数=
| 1 |
| 2 |
③三氯化硼中的硼为sp2杂化,无孤对电子,分子中键与键之间的夹角为120°,是平面三角形结构,空间结构对称属于非极性分子,故正确;
④三氯化硼是平面三角形结构,CH2O的分子结构为平面三角形,则二者分子空间结构类似,故正确.
故选C.
点评:本题考查原子轨道杂化,分子立体构型等,难度适中,注意三氯化硼中的硼为sp2杂化,无孤对电子,分子中键与键之间的夹角为120°,是平面三角形结构.

练习册系列答案
相关题目
下列每组中各有3对物质,它们都能用分液漏斗分离的是( )
①乙酸乙酯和水、乙醇和水、苯酚和水
②二溴乙烷和水、溴苯和水、硝基苯的水
③甘油和水、乙醛的水、乙酸和乙醇
④油酸和水、甲苯和水、已烷和水.
①乙酸乙酯和水、乙醇和水、苯酚和水
②二溴乙烷和水、溴苯和水、硝基苯的水
③甘油和水、乙醛的水、乙酸和乙醇
④油酸和水、甲苯和水、已烷和水.
| A、④ | B、② | C、①③ | D、②④ |
下列离子方程式书写正确的是( )
| A、少量的金属钠投入水中:2Na+2H2O═2Na++2OH-+H2↑ |
| B、铝片投入稀盐酸中:Al+6H+═Al3++3H2↑ |
| C、氢氧化钡溶液与稀硫酸混合:Ba2++SO42-═BaSO4↓ |
| D、氧化铝溶于烧碱溶液:Al2O3+2OH-═AlO2-+H2O |
有机物X、Y、M(M为乙酸)的转化关系为:,淀粉→X→Y
乙酸乙酯,下列说法错误的是( )
| M |
| A、X可用新制的氢氧化铜检验 |
| B、反应X→Y中,1molX可生成3molY |
| C、由Y生成乙酸乙酯的反应属于取代反应 |
| D、可用碘的四氯化碳溶液检验淀粉是否水解完全 |
有关实验操作或实验突发事件处理正确的是( )
| A、用10mL量筒量取8.58mL蒸馏水 |
| B、将氢氧化钠固体直接放在称量纸上称量 |
| C、中和滴定时,滴定管用蒸馏水洗净后直接装入标准盐酸溶液 |
| D、不慎将苯酚溶液沾到皮肤上,立即用酒精清洗 |
下列各反应的离子方程式中,错误的是( )
A、硫酸铝溶液中加入过量的氨水:Al3++4NH3?H2O═AlO
| ||||
| B、澄清石灰水与少量小苏打溶液混合:Ca2+十OH-+HCO3-=CaCO3↓+H2O | ||||
C、铁片放入过量的稀硝酸中:3Fe+8H++2NO
| ||||
D、偏铝酸钠与过量盐酸反应:AlO
|
用NA表示阿伏加德罗常数的值,下列叙述正确的是( )
| A、1mol Na2O2固体中含离子总数为4NA | ||
| B、标准状况下,22.4L己烷中共价键数目为19NA | ||
| C、由乙烯和环己烷组成的混合物28g,含电子数为16NA | ||
D、1L浓度为1mol/L的Na2CO3溶液中含有的
|
实验室的钠着火燃烧时,可用下列哪种物质灭火( )
| A、水 | B、沙土 |
| C、泡沫灭火器 | D、干粉灭火器 |
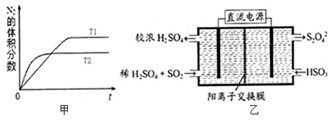 为有效控制雾霾,各地积极采取措施改善大气质量,研究并有效控制空气中的氮氧化物、碳氧化物和硫氧化物含量显得尤为重要.
为有效控制雾霾,各地积极采取措施改善大气质量,研究并有效控制空气中的氮氧化物、碳氧化物和硫氧化物含量显得尤为重要.