题目内容
4.制备氮化镁的装置示意图如下:
回答下列问题:
(1)仪器a的名称是分液漏斗,b的名称是圆底烧瓶.
(2)写出NaNO2和(NH4)2SO4反应制备氮气的化学方程式:(NH4)2SO4+2NaNO2$\frac{\underline{\;\;△\;\;}}{\;}$2N2↑+Na2SO4+4H2O.
(3)C的作用是除去空气中的氧气.
(4)写出E中发生反应的化学方程式:N2+3Mg$\frac{\underline{\;\;△\;\;}}{\;}$Mg3N2.
(5)请用化学方法确定氮化镁是否含有未反应的镁,写出实验操作及现象取少量产物于试管中,加入少量蒸馏水,试管底部有沉淀生成,弃去上层清液,加入盐酸,若观察到有气泡产生,则证明产物中含有未反应的镁.
分析 由图可知仪器的名称,A中发生(NH4)2SO4+2NaNO2$\frac{\underline{\;\;△\;\;}}{\;}$2N2↑+Na2SO4+4H2O,C中硫酸亚铁溶液可除去空气中的氧气,D中浓硫酸干燥氮气,E中发生N2+3Mg$\frac{\underline{\;\;△\;\;}}{\;}$Mg3N2,F可防止倒吸,G中硫酸亚铁溶液可防止空气中的氧气进入E中,以此来解答.
解答 解:(1)仪器a的名称是分液漏斗,b的名称是圆底烧瓶,故答案为:分液漏斗;圆底烧瓶;
(2)NaNO2和(NH4)2SO4反应制备氮气的化学方程式为(NH4)2SO4+2NaNO2$\frac{\underline{\;\;△\;\;}}{\;}$2N2↑+Na2SO4+4H2O,
故答案为:(NH4)2SO4+2NaNO2$\frac{\underline{\;\;△\;\;}}{\;}$2N2↑+Na2SO4+4H2O;
(3)C的作用为除去空气中的氧气,防止Mg与氧气反应,故答案为:除去空气中的氧气;
(4)E中发生反应的化学方程式为N2+3Mg$\frac{\underline{\;\;△\;\;}}{\;}$Mg3N2,故答案为:N2+3Mg$\frac{\underline{\;\;△\;\;}}{\;}$Mg3N2;
(5)因氮化镁与水反应,Mg不溶于水,但Mg与酸反应,则确定氮化镁是否含有未反应的镁,其实验操作及现象为取少量产物于试管中,加入少量蒸馏水,试管底部有沉淀生成,弃去上层清液,加入盐酸,若观察到有气泡产生,则证明产物中含有未反应的镁,
故答案为:取少量产物于试管中,加入少量蒸馏水,试管底部有沉淀生成,弃去上层清液,加入盐酸,若观察到有气泡产生,则证明产物中含有未反应的镁.
点评 本题考查物质的制备实验,为高频考点,把握实验装置的作用、发生的反应及制备原理为解答的关键,侧重分析与实验能力的考查,注意物质性质的综合应用,题目难度不大.

 名校课堂系列答案
名校课堂系列答案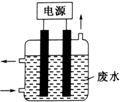 用如图所示装置除去含CN-、Cl-废水中的CN-时,控制溶液PH为9~10,阳极产生的ClO-将CN-氧化为两种无污染的气体,下列说法不正确的是( )
用如图所示装置除去含CN-、Cl-废水中的CN-时,控制溶液PH为9~10,阳极产生的ClO-将CN-氧化为两种无污染的气体,下列说法不正确的是( )| A. | ClO-将CN-氧化过程中,每消耗1molCN-转移10mol电子 | |
| B. | 阳极的电极反应式为:Cl-+2OH--2e-═ClO-+H2O | |
| C. | 阴极的电极反应式为:2H2O+2e-═H2↑+2OH- | |
| D. | 在电解过程中,废水中CN-和Cl-均移向阳极 |
| A. | 氢氧化铁溶于氢碘酸中:2Fe(OH)3+6H++2I-═2Fe2++I2+6H2O | |
| B. | 向Na2SiO3溶液中通入过量SO2:SiO32-+SO2+H2O═H2SiO3↓+SO32- | |
| C. | 向0.3mol/LNaClO溶液中滴加等体积的0.2mol/LNaHSO3溶液:2HSO3-+4ClO-═2SO42-+2Cl-+2HClO | |
| D. | 向碘化亚铁溶液中滴加溴的四氯化碳溶液2Br2+2Fe2++2I-═I2+4Br-+2Fe3+ |
| A. | 室温下测定等浓度氨水和NaOH溶液的pH,比较氨水和NaOH碱性强弱 | |
| B. | 将氨水缓慢滴入AlCl3溶液中,研究Al(OH)3的两性 | |
| C. | 将蘸有浓氨水和浓硫酸的玻璃棒靠近,观察到白烟 | |
| D. | 加热除去NH4Cl中的少量NaHC03 |
| A. | 聚乙烯能使高锰酸钾酸性溶液变色 | |
| B. | 等物质的量的甲烷、乙炔完全燃烧,耗氧量甲烷大 | |
| C. | 葡萄糖、氨基酸在一定条件下都能发生酯化反应 | |
| D. | 分子式为C2H4、C3H6、C4H8的三种烃肯定是同系物 |
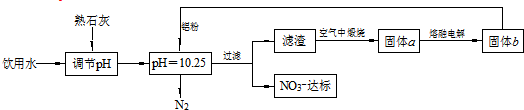
下列说法不正确的是( )
| A. | 该方案在调节pH时,若pH过大或过小都会造成Al的利用率降低 | |
| B. | 为了降低能耗,工业上往往用AlCl3代替固体a来制备固体b | |
| C. | 用熟石灰调节PH主要原因是价格便宜且引入的Ca2+对人体无害 | |
| D. | 在加入铝粉的反应中,氧化产物和还原产物的物质的量之比为10:3 |
| A. | 0.1mol/L的硫酸铵溶液中:c(NH4+)>c(SO42-)>c(H+) | |
| B. | 室温下,pH=7的醋酸和醋酸钠的混合溶液中:c(CH3COO-)>c(Na+) | |
| C. | 将水加热到100℃,pH=6:c(H+)>c(OH-) | |
| D. | 同浓度的三种溶液:①CH3COONH4 ②NH4Cl ③NH3•H2O中,c(NH4+)由大到小的顺序是②③① |
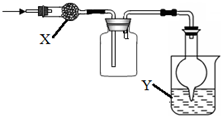 如图是用于干燥、收集并吸收多余气体的装置,下列方案正确的是( )
如图是用于干燥、收集并吸收多余气体的装置,下列方案正确的是( )