题目内容
在标准状况下,3L CH4,2L C2H6与100L空气完全燃烧后,恢复到原状态,此时所得气体的体积应是 .
考点:化学方程式的有关计算
专题:计算题
分析:根据甲烷和乙烷燃烧的化学方程式确定消耗氧气的量以及生成的气体的量,进而计算最终气体的量.
解答:
解:空气中氧气的体积百分比是21%,大约为1/5,所以100L空气中有20L氧气,CH4+2O2
CO2+2H2O,2C2H6+7O2
6H2O+4CO2,所以标准状况下,3L的CH4需要6L的O2,得到3L的CO2;2L的C2H6需要7L的O2,得到4L的CO2.
故所得气体的体积为100-6-7+3+4,故答案为:94.
| ||
| ||
故所得气体的体积为100-6-7+3+4,故答案为:94.
点评:本题考查学生烷烃的燃烧规律以及方程式的意义,注意基础知识的掌握,难度不大.

练习册系列答案
相关题目
下列有机物检验方法正确的是( )
| A、取少量卤代烃加入NaOH水溶液共热,冷却,再加入AgNO3溶液检验卤代烃中卤原子的存在 |
| B、淀粉用酸催化水解后的溶液加入新制银氨溶液,水浴加热,来检验葡萄糖 |
| C、通过红外光谱分析可以区分乙醇和乙酸乙酯 |
| D、用新制CaO检验乙醇中是否含有水分 |
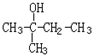 此化合物在浓硫酸作用下发生消去反应,写出所有可能的有机产物的结构简式:
此化合物在浓硫酸作用下发生消去反应,写出所有可能的有机产物的结构简式: