题目内容
下列离子组在指定溶液中能大量共存的是( )
| A、澄清透明的溶液中:Cu2+、K+、SO42-、S2- |
| B、加入苯酚显紫色的溶液:K+、NH4+、Cl-、SCN- |
| C、1.0 mol?L-1的KNO3溶液中:Na+、Fe2+、Cl-、SO42- |
| D、能溶解Al2O3的溶液中:Mg2+、Fe3+、AlO2-、HCO3- |
考点:离子共存问题
专题:离子反应专题
分析:A.Cu2+、S2-反应生成沉淀;
B.加入苯酚显紫色的溶液含有Fe3+;
C.离子之间不发生反应;
D.能溶解Al2O3的溶液呈强酸性或强碱性.
B.加入苯酚显紫色的溶液含有Fe3+;
C.离子之间不发生反应;
D.能溶解Al2O3的溶液呈强酸性或强碱性.
解答:
解:A.Cu2+、S2-反应生成CuS沉淀,不能大量共存,故A错误;
B.加入苯酚显紫色的溶液含有Fe3+,与SCN-反应而不能大量共存,故B错误;
C.离子之间不发生反应,可大量共存,故C错误;
D.能溶解Al2O3的溶液呈强酸性或强碱性,无论溶液呈酸性还是碱性,HCO3-都不能大量共存,且Mg2+、Fe3+与AlO2-发生互促水解,故D错误.
故选C.
B.加入苯酚显紫色的溶液含有Fe3+,与SCN-反应而不能大量共存,故B错误;
C.离子之间不发生反应,可大量共存,故C错误;
D.能溶解Al2O3的溶液呈强酸性或强碱性,无论溶液呈酸性还是碱性,HCO3-都不能大量共存,且Mg2+、Fe3+与AlO2-发生互促水解,故D错误.
故选C.
点评:本题考查离子的共存,为高考常见题型,侧重信息的抽取和氧化还原反应及水解反应的考查,注重学生思维严密性的训练,有利于提高学生分析问题解决问题的能力,题目难度不大.

练习册系列答案
相关题目
下列有关厨房中铝制品的使用中,你认为合理的是( )
| A、盛放食醋 |
| B、烧煮开水 |
| C、用金属丝擦表面的污垢 |
| D、用碱溶液洗涤 |
将氨水缓缓地滴入盐酸中至中性,下列有关的说法:①盐酸过量 ②氨水过量 ③恰好完全反应 ④c (NH4+)=c(Cl-) ⑤c (NH4+)<c(Cl-) 正确的是( )
| A、②④ | B、③④ | C、②⑤ | D、①⑤ |
下列各组物质中,前一种是化合物,后一种是混合物的是( )
| A、铝土矿,洁净的雨水 |
| B、蒸馏水,粗盐 |
| C、氢氧化钾,含铜80%的氧化铜 |
| D、红磷,空气 |
能与Fe3+反应,且能证明Fe3+具有氧化性的试剂是( )
①SCN-;②Fe;③Fe2+;④Cu;⑤H2S;⑥OH-.
①SCN-;②Fe;③Fe2+;④Cu;⑤H2S;⑥OH-.
| A、①②③ | B、②④⑤ |
| C、①③⑥ | D、①②⑤ |
在密闭容器中进行反应:2A(g)+B(g)?3C(g)△H>0.下列各图表示当其他条件不变时,改变某一条件对上述反应的影响,其中分析正确的是( )
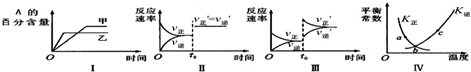

| A、图I表示温度对化学平衡的影响,且甲的温度较高 |
| B、图Ⅱ表示t0时刻缩小容器体积对反应速率的影响 |
| C、图Ⅲ表示t0时刻增大B浓度对反应速率的影响 |
| D、图Ⅳ中a、b、c三点中只有b点已经达到化学平衡状态 |
