题目内容
5℃时,弱酸的电离平衡常数如下表,下列说法正确的是( )
| 弱酸化学式 | CH3COOH | HCN | H2CO3 |
| 电离平衡常数 | 1.8×10-5 | 4.9×10-10 | K1=4.3×10-7 K2=5.6×10-11 |
| A、等pH的溶液物质的量浓度关系:C(NaCN)>C(Na2CO3)>C(CH3COONa) |
| B、amol/L HCN与b mol/LNaOH溶液等体积混合后所得溶液中c(Na+)>c(CN-),则a一定小于b |
| C、相同体积相同浓度的NaCN 和CH3COONa溶液中,NaCN溶液的离子总数少 |
| D、HCN+CO32-→CN-+H2O+CO2↑ |
考点:弱电解质在水溶液中的电离平衡
专题:
分析:弱酸的电离平衡常数越大,其酸性越强,等pH的弱酸溶液,酸性越强的酸其物质的量浓度越小,弱酸根离子水解程度越小,结合强酸能和弱酸盐反应制取弱酸分析解答.
解答:
解:根据电离平衡常数知,酸性强弱顺序为:HCOOH>H2CO3>HCN>HCO3-,
A、弱酸的酸性越弱,其离子水解程度越大,等pH的溶液物质的量浓度关系:c(CH3COONa)>c(NaCN)>c(Na2CO3),故A错误;
B、amol/L HCN与b mol/LNaOH溶液等体积混合后所得溶液中c(Na+)>c(CN-),说明溶液显碱性,NaCN溶液显碱性,a=b,故B错误;
C、根据电荷守恒,c(CH3COO-)+c(OH-)=c(Na+)+c(H+),c(CN-)+c(OH-)=c(Na+)+c(H+),即离子总数是n(Na+ )+n(H+)的2倍,而NaCN的水解程度大,即NaCN溶液中的c(OH-)大,c(H+)小,c(Na+)相同,所以乙酸钠中离子浓度大,故C正确;
D、酸性强弱顺序为:HCOOH>H2CO3>HCN>HCO3-,所以HCN+CO32-=CN-+HCO3-,故D错误;
故选C.
A、弱酸的酸性越弱,其离子水解程度越大,等pH的溶液物质的量浓度关系:c(CH3COONa)>c(NaCN)>c(Na2CO3),故A错误;
B、amol/L HCN与b mol/LNaOH溶液等体积混合后所得溶液中c(Na+)>c(CN-),说明溶液显碱性,NaCN溶液显碱性,a=b,故B错误;
C、根据电荷守恒,c(CH3COO-)+c(OH-)=c(Na+)+c(H+),c(CN-)+c(OH-)=c(Na+)+c(H+),即离子总数是n(Na+ )+n(H+)的2倍,而NaCN的水解程度大,即NaCN溶液中的c(OH-)大,c(H+)小,c(Na+)相同,所以乙酸钠中离子浓度大,故C正确;
D、酸性强弱顺序为:HCOOH>H2CO3>HCN>HCO3-,所以HCN+CO32-=CN-+HCO3-,故D错误;
故选C.
点评:本题考查弱电解质的电离,根据平衡常数确定酸性强弱,从而确定酸之间的转化,结合电荷守恒来分析解答,难度中等.

练习册系列答案
 单元期中期末卷系列答案
单元期中期末卷系列答案
相关题目
下列物质中分子内和分子间均可形成氢键的是( )
| A、NH3 |
B、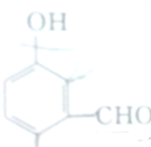 |
| C、H2S |
| D、C2H5OH |
常温时,①pH=2的CH3COOH溶液; ②pH=2的HCl溶液; ③pH=12的氨水;④pH=12的NaOH溶液.相同条件下,有关上述溶液的比较中,不正确的是( )
| A、由水电离的c(H+):①=②=③=④ |
| B、等体积的①、②、④溶液分别与足量铝粉反应,生成H2的量:②最大 |
| C、将②、③溶液混合后,pH=7,消耗溶液的体积:②>③ |
| D、向溶液中加入100mL水后,溶液的pH:③>④>②>① |
下列对表中各种烃的说法中正确的是( )
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 |
| CH4 | C3H6 | C5H8 | C2H6 | C4H8 | C3H8 | C5H10 | C7H12 |
| A、1、4、7对应的烃互为同系物,2、5、8对应的烃互为同系物 |
| B、第6种烃与等物质的量的溴加成,所得产物有2种,则该烃的结构有4种(不考虑顺反异构) |
| C、第8种烃一定能使酸性高锰酸钾溶液褪色 |
| D、1、4、7对应的烃中碳的质量分数逐渐减小 |
中国科学家利用干冰和金属钠在不锈钢反应釜中反应合成出微米级金刚石,其反应为CO2(s)+Na
金刚石+石墨+Na2CO3.下列说法不正确的是( )
| 440℃ |
| A、金刚石与石墨互为同素异形体 |
| B、11.5 g金属钠的物质的量为0.5 mol |
| C、44 g CO2在标准状况下的体积为22.4 L |
| D、Na2CO3的摩尔质量为106 g |

 +CH3COOH→
+CH3COOH→ 聚合物
聚合物 可用于制备高吸水性树脂,其单体的结构简式为
可用于制备高吸水性树脂,其单体的结构简式为 某学生在A、B、C、D四只小烧瓶中分别放入:干燥的细铁丝;浸过食盐水的细铁丝;浸过清水的细铁丝.然后装配成如图所示的四套装置,每隔一段时间测量导管中水面上升的高度,结果如表(表中所列数据为导管中水面上升的高度/cm)
某学生在A、B、C、D四只小烧瓶中分别放入:干燥的细铁丝;浸过食盐水的细铁丝;浸过清水的细铁丝.然后装配成如图所示的四套装置,每隔一段时间测量导管中水面上升的高度,结果如表(表中所列数据为导管中水面上升的高度/cm)