题目内容
1.某种苯的同系物0.1mol完全燃烧,生成的气体通过浓H2SO4后,使浓H2SO4增重10.8g,此种苯的同系物在苯环上的一溴取代物只有一种,则苯的同系物的分子式为C9H12,结构简式为 .
.
分析 苯的同系物组成通式为CnH2n-6,将燃烧产生高温气体通过浓硫酸增重10.8g为水的质量,根据n=$\frac{m}{M}$计算出水的物质的量,再根据质量守恒计算出该有机物分子中含有H原子数,从而可知其分子式;该苯的同系物苯环上的一溴代物只有一种,说明苯环上只有1种H原子,再结合分子式确定可能的结构简式.
解答 解:苯的同系物在足量的氧气中完全燃烧,将燃烧产生高温气体通过浓硫酸增重10.8g为水的质量,水的物质的量为:$\frac{10.8g}{18g/mol}$=0.6mol,
则该苯的同系物中含有H原子数为:N(H)=$\frac{0.6mol×2}{0.1mol}$=12,苯同系物的组成通式为CnH2n-6,则2n-6=12,解得n=9,
所以该苯的同系物的分子式为:C9H12,
该苯的同系物苯环上的一溴代物只有一种,说明苯环上只有1种H原子,该苯同系物的结构简式为: ,
,
故答案为:C9H12; .
.
点评 本题考查有机物分子式与结构的确定,题目难度不大,明确苯同系物的组成通式为解答关键,注意掌握常见有机物结构与性质,试题培养了学生的分析能力及化学计算能力.

练习册系列答案
相关题目
11.下列物质中,属于“城市空气质量日报”报道的污染物是( )
| A. | N2 | B. | O2 | C. | CO2 | D. | SO2 |
9.下列实验,温度计水银球不能放在液体中的是( )
| A. | 石油分馏实验 | B. | 乙醇脱水实验 | C. | 制溴苯 | D. | 苯的硝化实验 |
16.下列有机分子中,所有的原子不可能处于同一平面的是( )
| A. | CH2=CH-C≡N | B. | CH2=CH-CH=CH2 | C. |  | D. | 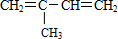 |
6.LiFePO4新型锂离子动力电池以其独特的优势成为奥运会绿色能源的新宠.已知该电池放电时的电极反应式为:正极 FePO4+Li++e-═LiFePO4; 负极 Li-e-═Li+ 下列说法中正确的是( )
| A. | 充电时电池反应为FePO4+Li═LiFePO4 | |
| B. | 充电时动力电池上标注“+”的电极应与外接电源的负极相连 | |
| C. | 放电时电池内部Li+向正极移动 | |
| D. | 放电时,在正极上是Li+得电子被还原 |
13.下列化合物不能通过化合反应获得的是( )
| A. | Fe(OH)3 | B. | CaSiO3 | C. | Al(OH)3 | D. | NaHCO3 |
10.下列说法正确的是( )
| A. | HClO2→ClO2+Cl2+H2O(未配平),1 mol HClO2分解时转移电子的物质的量为1 mol | |
| B. | 标准状况下,28 g CO、C2H4混合气体与22.4 L N2所含有的分子数都是NA | |
| C. | 与金属Cu常温下反应放出气体的溶液可以存在的离子有:Fe2+、Al3+、SO42-、K+ | |
| D. | 在燃煤时加入适量石灰石,可减少SO2的排放,其中发生的反应为:2CaCO3+O2+2SO2$\frac{\underline{\;高温\;}}{\;}$2CaSO3+2CO2 |
16.在0.5L的密闭容器中,一定量的H2和N2进行如下化学反应:3H2(g)+N2(g)═2NH3(g)△H<0,其化学平衡常数K与温度t的关系如下表.请回答下列问题.
①比较K1,K2的大小,K1>K2(填写“>”、“=”或“<”).
②在400℃时,当测得NH3和N2、H2的物质的量分别为3mol和1mol、2mol时,则该反应的 V(H2)正> V (H2)逆(填写“>”、“=”或“<”).
| t/℃ | 200 | 300 | 400 |
| K | K1 | K2 | 0.5 |
②在400℃时,当测得NH3和N2、H2的物质的量分别为3mol和1mol、2mol时,则该反应的 V(H2)正> V (H2)逆(填写“>”、“=”或“<”).