题目内容
19.下列说法中正确的是( )| A. | 由反应:2Fe2++Cl2→2Fe3++2Cl-,可以得出还原性Cl2<Fe3+ | |
| B. | 由于钢铁表面水膜里溶有氧气和二氧化碳,所以日常的金属腐蚀以析氢腐蚀为主 | |
| C. | 将钢铁接在外电源的负极上,另一金属(不是惰性金属)接在外电源的正极上组成电解池,可以防钢铁腐蚀 | |
| D. | 纯锌与稀硫酸反应比不纯的锌(一般含铁、铜等杂质)与相同的稀硫酸反应慢 |
分析 A、反应:2Fe2++Cl2→2Fe3++2Cl-中,氯气是氧化剂;
B、日常的金属腐蚀以吸氧腐蚀为主;
C、电解池的阴极能有效防止金属的腐蚀;
D、构成原电池加快化学反应速率.
解答 解:A、反应:2Fe2++Cl2→2Fe3++2Cl-中,氯气是氧化剂,根据强制弱,可知氧化性Cl2>Fe3+,故A错误;
B、日常的金属腐蚀以吸氧腐蚀为主,而不是析氢腐蚀,故B错误;
C、电解池的阴极能有效防止金属的腐蚀,所以将钢铁接在外电源的负极上,也就是阴极,能防钢铁腐蚀,故C正确;
D、构成原电池加快化学反应速率,所以不纯的锌与相同的稀硫酸反应快,故D正确;
故选CD.
点评 本题考查了原电池原理和电解池原理的应用,注意把握金属的电化学腐蚀和防护原理,题目难度不大.

练习册系列答案
相关题目
7.砹(At)是原子序数最大的卤族元素,推测砹及其化合物最不可能具有的性质是( )
| A. | 砹是有色固体 | B. | 砹易溶于有机溶剂 | ||
| C. | H2很难与砹化合 | D. | HAt比HCl稳定 |
14.下列物质中,能与醋酸发生反应的是( )
①石蕊②乙醇③氢氧化钠④铝⑤氧化镁⑥碳酸钙.
①石蕊②乙醇③氢氧化钠④铝⑤氧化镁⑥碳酸钙.
| A. | ①③④⑤⑥ | B. | ②③④⑤ | C. | ①②④⑤⑥ | D. | 全部 |
4.①②③④四种金属片两两相连浸入稀硫酸中都可组成原电池.①②相连时,外电路电子从①流向②;①③相连时,①为负极;②④相连时,②上有气泡逸出;③④相连时,③不断溶解.据此判断这四种金属活动性由大到小的顺序是( )
| A. | ①③④② | B. | ①③②④ | C. | ③④②① | D. | ③①②④ |
11.下列关于卤代烃的叙述正确的是( )
| A. | 所有卤代烃是难溶于水,比水重的液体 | |
| B. | 所有卤代烃在适当条件下都能发生消去反应 | |
| C. | 所有卤代烃都含有卤素原子 | |
| D. | 所有卤代烃都是通过取代反应制得的 |
9.化学科学需要借助化学专用语言描述,下列有关化学用语正确的是( )
| A. | 镁离子的电子式Mg2+ | B. | Cl的结构示意图 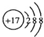 | ||
| C. | 氯离子的电子式Cl- | D. | 质量数为37的氯原子${\;}_{37}^{17}$Cl |
 (1)为了做到合理营养,我国营养学家将食物分为A、B、C、D、E五类,请回答下列问题:①营养学家将这五类形象地设计成图示的“平衡膳食宝塔”,并提倡居民每天均衡地吃这五类食物.为保证身体健康,建议在每日摄入的总能量中,早、中、晚餐的能量比例是3:4:3.
(1)为了做到合理营养,我国营养学家将食物分为A、B、C、D、E五类,请回答下列问题:①营养学家将这五类形象地设计成图示的“平衡膳食宝塔”,并提倡居民每天均衡地吃这五类食物.为保证身体健康,建议在每日摄入的总能量中,早、中、晚餐的能量比例是3:4:3.