题目内容
14.用FeS2纳米材料制成的高容量锂电池,电极分别是二硫化亚铁和金属锂,电解液是含锂盐的有机溶剂.下列说法错误的是( )| A. | 金属锂作电池的负极 | |
| B. | 电池正极反应为FeS2+4Li++4e-═Fe+2Li2S | |
| C. | 放电时,Li+向负极迁移 | |
| D. | 电池总反应为FeS2+4Li═Fe+2Li2S |
分析 高容量锂电池,电极分别是二硫化亚铁和金属锂,电解液是含锂盐的有机溶剂,则Li为负极,失去电子发生氧化反应,二硫化亚铁为正极,得到电子发生还原反应,原电池中阳离子向正极移动,以此来解答.
解答 解:A.Li失去电子,作负极,故A正确;
B.二硫化亚铁为正极,得到电子发生还原反应,正极反应为FeS2+4Li++4e-═Fe+2Li2S,故B正确;
C.放电时,Li+向正极迁移,故C错误;
D.Li失去电子,Fe得到电子,电池总反应为FeS2+4Li═Fe+2Li2S,故D正确;
故选C.
点评 本题考查原电池,为高频考点,把握Li为负极及电极反应为解答本题的关键,侧重分析与应用能力的考查,注意原电池的工作原理及应用,题目难度不大.

练习册系列答案
相关题目
4.下列有关物质性质排列顺序正确的是( )
| A. | 沸点:NH3>H2O>H2S | |
| B. | 酸性:H2SO4>HClO4>H3PO3 | |
| C. | 结合质子的能力:CO32->ClO->CH3COO- | |
| D. | 气态氢化物的热稳定性:H2O>HF>NH3 |
5.现有CuO和Fe3O4的混合物7.6g,向其中加入1mol.L-l的H2SO4溶液100mL恰好完全反应,若将15.2g该混合物用足量CO还原,充分反应后剩余固体质量为( )
| A. | 13.6g | B. | 12g | C. | 6g | D. | 3.2g |
2.乌洛托品在工业生产中有广泛用途,其结构式如图所示.下列说法正确的是( )
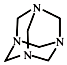

| A. | 化学式为C6H12N4,属于饱和烃 | |
| B. | 不能发生加成反应,一氯取代产物有3种 | |
| C. | 分子中既含极性共价键又含非极性共价键 | |
| D. | 可由甲醛(HCHO)与氨气按物质的量之比3:2完全反应制得 |
4.工业上用Fe2(SO4)3酸性溶液处理SO2废气的工艺流程如图,下列说法不正确的是( )

| A. | 溶液的pH:①>②>③ | |
| B. | 整个过程中Fe2(SO4)3溶液可以循环利用 | |
| C. | 溶液②转化为溶液③发生反应的离子方程式为4H++4Fe2++O2=4Fe3++2H2O | |
| D. | 向②溶液中滴加KSCN溶液,溶液可能变为血红色 |
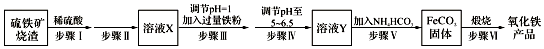
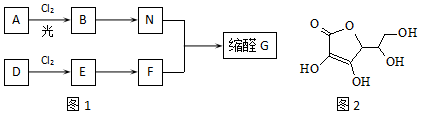
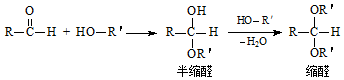
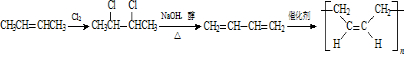
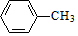 ,E的名称是1,2-二氯乙烷.
,E的名称是1,2-二氯乙烷.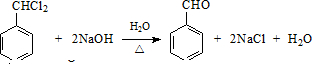 .
.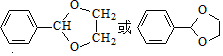 .G有多种同分异构体,写出其中能同时满足以下条件的所有同分异构体的结构简式:
.G有多种同分异构体,写出其中能同时满足以下条件的所有同分异构体的结构简式: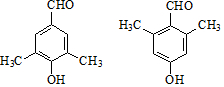 .
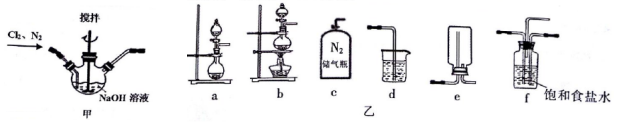
. .
.
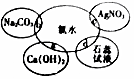 氯水具有多种性质,根据新制氯水分别与如图四种物质发生的反应填空(已知反应中氯水足量)
氯水具有多种性质,根据新制氯水分别与如图四种物质发生的反应填空(已知反应中氯水足量)