题目内容
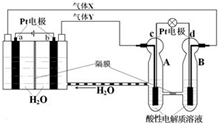 “天宫一号”的供电系统( RFC)是一种将水电解技术与氢氧燃料电池技术相结合的可充放电池.如图所示为RFC工作原理示意图,有关说法正确的是( )
“天宫一号”的供电系统( RFC)是一种将水电解技术与氢氧燃料电池技术相结合的可充放电池.如图所示为RFC工作原理示意图,有关说法正确的是( )| A、当有0.1 mol电子转移时,a极产生1.12 L H2 |
| B、b极上发生的电极反应是:4H2O+4e-=2H2↑+4OH- |
| C、d极上发生的电极反应是:O2+4H++4e-=2H2O |
| D、c极上发生还原反应,B中的H+通过隔膜进入A |
考点:原电池和电解池的工作原理
专题:
分析:依据图示知左边装置是电解池,右边装置是原电池,ab电极是电解池的电极,由电源判断a为阴极产生的气体X是氢气,b为阳极产生的气体Y是氧气;cd电极是原电池的正负极,c是正极,d是负极;电解池中的电极反应为:b电极为阳极失电子发生氧化反应:4OH--4e-=2H2O+O2↑;a电极为阴极得到电子发生还原反应:4H++4e-=2H2↑;原电池中是酸性溶液,电极反应为:d为负极失电子发生氧化反应:2H2-4e-=4H+;c电极为正极得到电子发生还原反应:O2+4H++4e-=2H2O,结合电极上的电子守恒分析计算.
解答:
解:A、当有0.1 mol电子转移时,a电极为原电池正极,电极反应为4H++4e-=2H2↑,产生0.05mol即标准状况下1.12LH2,没有说明标准状况,气体体积不一定是1.12L,故A错误;
B、依据图示,b电极为阳极失电子发生氧化反应:4OH--4e-=2H2O+O2↑,故B错误;
C、d为负极,氢气失电子发生氧化反应,2H2-4e-=4H+,故C错误;
D.c电极为正极,氧气在正极上得到电子发生还原反应:O2+4H++4e-=2H2O,右端装置B池中的H+可以通过隔膜进入A池,故D正确;
故选D.
B、依据图示,b电极为阳极失电子发生氧化反应:4OH--4e-=2H2O+O2↑,故B错误;
C、d为负极,氢气失电子发生氧化反应,2H2-4e-=4H+,故C错误;
D.c电极为正极,氧气在正极上得到电子发生还原反应:O2+4H++4e-=2H2O,右端装置B池中的H+可以通过隔膜进入A池,故D正确;
故选D.
点评:本题考查了化学电源新型电池,主要考查原电池和电解池的工作原理、电极判断、电极反应,注意原电池中电解质溶液是酸而不是碱,电极反应式的书写是易错点.

练习册系列答案
相关题目
下列各组中粒子在指定溶液中能大量共存的是( )
| A、0.lmol.L-1氯化铁溶液中Ca2+、Ba2+、Na+、HCO3- | ||
| B、氯水中 H2SO3、K+、SO42-、NH4+ | ||
| C、与镁反应只产生氢气的溶液中 NO3-、C1-、H+、A13+ | ||
D、
|
在强酸性无色透明溶液中,下列各组离子不能大量共存的是( )
| A、Fe3+、K+、Cl-、MnO4- |
| B、K+、Na+、NO3-、Cl- |
| C、Zn2+、Al3+、SO42-、Cl- |
| D、Ba2+、NH4+、Cl-、NO3- |
下列各组物质中分子数相同的是( )
| A、2 L CO和2 L CO2 |
| B、9 g H2O和标准状况下11.2 L CO2 |
| C、标准状况下1 mol O2和22.4 L H2O |
| D、0.2 mol H2和4.48 L HCl气体 |
下列叙述正确的是( )
| A、乙醇的结构简式为:C2H6O |
B、硫离子的结构示意图为: |
| C、NaHCO3电离:NaHCO3=Na++H++CO32- |
D、氮分子的结构式为: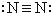 |
设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A、在常温、常压下,11.2 L N2含有的分子数为0.5 NA |
| B、标准状况下,22.4 L H2和O2的混合物所含分子数为NA |
| C、标准状况下,18 g H2O的体积是22.4 L |
| D、1 mol SO2的体积是22.4 L |
下列说法中正确的是( )
| A、KOH的摩尔质量是56 g |
| B、1 mol H2O的质量是18 g/mol |
| C、Cl2的摩尔质量是35.5 g/mol |
| D、1 mol N2的质量是28 g |
化学知识在生产和生活中有着重要的应用.下列说法中,错误的是( )
| A、浓硝酸具有强氧化性,可用铁罐贮运浓硝酸 |
| B、明矾常作为净水剂,双氧水通常可用于作杀菌消毒 |
| C、合成氨工业中通过升高温度可以增大平衡常数K,来提高氨的产率 |
| D、催化剂可以改变反应速率,对平衡移动没有影响 |