题目内容
17.关于下列图示的说法中,正确的是( )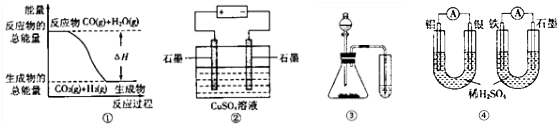
| A. | 图①表示可逆反应:CO(g)+H2O(g)?CO2(g)+H2(g)△H>0 | |
| B. | 图②为电解硫酸铜溶液的装置,一段时间后,阴、阳两极有可能收集到相同体积的气体 | |
| C. | 图③实验装置可完成比较乙酸、碳酸、苯酚酸性强弱的试验 | |
| D. | 图④两个装置中个,通过导线的电子数相同时,消耗负极材料的物质的量也相同 |
分析 A、根据反应物的总能量和生成物的总能量的相对大小来判断该反应是吸热还是放热反应;
B、根据电解硫酸铜稀溶液,阳极开始生成氧气,阴极后产生氢气;
C、依据试剂加入顺序和反应现象对比比较,酸性强的生成酸性弱的分析;D、每个铝原子和铁原子失去电子数不等.
解答 解:A.图①反应物总能量大于生成物总能量,反应放热,则△H小于0,故A错误;
B.图②电解硫酸铜稀溶液,阳极开始生成氧气,阴极生成铜单质,铜离子电离完全后,阴极产生氢气,则阴、阳极产生气体体积之比可以等于1:1,故B正确;
C.分液漏斗中中的乙酸加入锥形瓶中的碳酸钠溶液反应生成气体,说明乙酸酸性强于碳酸,二氧化碳通入苯酚钠溶液变浑浊,说明碳酸酸性强于苯酚,故C正确;D.每个铝原子和铁原子失去电子数不等,所以两个装置是通过导线的电子数相等时,消耗的负极材料的物质的量不等,故D错误,故选BC.
点评 本题主要考查了化学反应类型(吸热还是放热)的判断,电解池中阴阳两极的判断、酸性强弱的比较以及原电池中电子得失守恒的应用等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
7.化学与人类生活密切相关,下列说法不正确的是( )
| A. | 化学可以识别、改变和创造分子 | |
| B. | 金刚石常用作砂纸、砂轮的磨料 | |
| C. | 氧化铁常用作红色油漆和涂料 | |
| D. | 葡萄糖可用于合成补钙药物及维生素C(结构如图)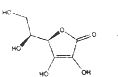 |
8.下列化学反应的有机生成物为纯净物的是( )
| A. | CH4和Cl2光照发生取代反应 | |
| B. | 1,3丁二烯与等物质的量的溴发生反应 | |
| C. | CH3CH(OH)CH2CH3在浓硫酸作用下加热的反应 | |
| D. | 乙烯和氯化氢加成 |
5.碘与氢气一定条件下反应的热化学方程式如下
(Ⅰ) I2(g)+H2(g)═2HI(g)△H=-9.48KJ/mol
(Ⅱ) I2(s)+H2(g)═2HI(g)△H=+26.48KJ/mol
下列判断正确的是( )
(Ⅰ) I2(g)+H2(g)═2HI(g)△H=-9.48KJ/mol
(Ⅱ) I2(s)+H2(g)═2HI(g)△H=+26.48KJ/mol
下列判断正确的是( )
| A. | 物质的量相同时,反应(Ⅰ)的反应物总能量比反应(Ⅱ)的反应物总能量高 | |
| B. | 反应(Ⅰ)和反应(Ⅱ)均为放热反应 | |
| C. | 反应(Ⅰ)的产物比反应(Ⅱ)的产物稳定 | |
| D. | 1mol H2(g)通入1mol I2中在该条件下反应的反应放热为9.48 kJ |
12.某两种气态烃组成的混合物,取其2.24L(标准状况下)充分燃烧,得到0.16mol二氧化碳气体和3.6g液态水.据此判断下列分析中不正确的是( )
| A. | 此混合气体中可能含有乙烷 | |
| B. | 此气体中一定含有甲烷 | |
| C. | 此混合气体中一定不含有丙烷 | |
| D. | 此气体若是乙烯与甲烷的混合气体,则甲烷与乙烯的体积比为2:3 |
2.下列关于反应“化合物甲+单质A$\stackrel{一定条件}{→}$化合物乙+单质B”的说法正确的是( )
| A. | 反应在水溶液中进行时,若A为金属,则B一定是金属 | |
| B. | 反应在水溶液中进行时,若A为非金属,则B一定是非金属 | |
| C. | 反应在加热或高温下进行时,若A为金属,则B一定是非金属 | |
| D. | 反应在加热或高温下进行时,若A为非金属,则B一定是金属 |
10.阿司匹林是日常生活中应用广泛的医药之一,它可由下列方法合成:
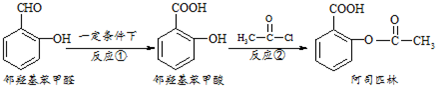
下列说法正确的是( )

下列说法正确的是( )
| A. | 与邻羟基苯甲酸互为同分异构体,苯环上一氯代物仅有2种且能发生银镜反应的酚类化合物共有3 种 | |
| B. | 用酸性KMnO4溶液直接氧化邻羟基苯甲醛可实现反应① | |
| C. | 邻羟基苯甲醛不能和溴水发生取代反应 | |
| D. | 1mol阿司匹林最多可以和2molNaOH反应 |
11.化学与科学技术、社会生活、环堍材料等密切相关.下列有关说法中错误的是( )
| A. | SO2是很好的抑菌剂,红酒中常加人微量的SO2 | |
| B. | 麦片中常加人微量铁粉,可以防止被氧化而变质 | |
| C. | “PM2.5“是指大气中直径≤2.5微米的颗粒物.其悬浮在空气中一定形成气溶胶 | |
| D. | 制饭勺、饭盒、高压锅等的不锈钢是合金 |
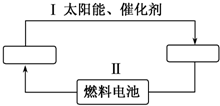 能源是21世纪极具发展前景的新能源之一,它既是绿色能源,又可循环使用.
能源是21世纪极具发展前景的新能源之一,它既是绿色能源,又可循环使用.