题目内容
12.写出下列电解质在水中电离的方程式(1)H2SO4H2SO4=2H++SO42- (2)H2OH2O?H++OH-(3)CH3COOHCH3COOH?CH3COO-+H+
(4)NH3•H2ONH3•H2O?NH4++OH-(5)NaHCO3NaHCO3=Na++HCO3-、HCO3-?H++CO32-.
分析 (1)硫酸为二元强酸,完全电离出氢离子和硫酸根离子;
(2)水为弱电解质,部分电离出氢离子和氢氧根离子;
(3)CH3COOH为弱电解质,部分电离出乙酸根离子和氢离子;
(4)一水合氨为弱碱,部分电离出铵根离子和氢氧根离子;
(5)碳酸氢钠为强电解质,完全电离,注意碳酸氢根离子为弱酸的酸式根离子不能拆,碳酸氢根离子部分电离.
解答 解:(1)H2SO4是强酸,属于强电解质,在溶液中完全电离,其电离方程式为:H2SO4=2H++SO42-,
故答案为:H2SO4=2H++SO42-;
(2)H2O是弱电解质,在水溶液里不能完全电离,电离方程式为:H2O?H++OH-,
故答案为:H2O?H++OH-;
(3)乙酸为弱电解质,部分电离,电离方程式:CH3COOH?CH3COO-+H+,
故答案为:CH3COOH?CH3COO-+H+;
(4)NH3•H2O为弱电解质,电离方程式为NH3•H2O?NH4++OH-,
故答案为:NH3•H2O?NH4++OH-;
(5)碳酸氢钠为强电解质,完全电离,电离方程式:NaHCO3═Na++HCO3-;碳酸氢根离子部分电离:NaHCO3=Na++HCO3-,
故答案为:NaHCO3=Na++HCO3-;HCO3-?H++CO32-.
点评 本题考查了电离方程式的书写,明确电解质的强弱及电离方程式的书写规则是解本题关键,注意原子团不能拆,强电解质在水溶液里完全电离生成阴阳离子,电离方程式写“=”,弱电解质在水溶液里部分电离,电离方程式写“?”,书写时要遵循原子守恒、电荷守恒,题目难度不大.

练习册系列答案
 互动课堂系列答案
互动课堂系列答案 激活思维智能训练课时导学练系列答案
激活思维智能训练课时导学练系列答案
相关题目
2.设NA为阿伏伽德罗常数的值,下列说法不正确的是( )
| A. | 34gH2O2含有的氢原子数为2NA | |
| B. | 0.1mol乙酸与0.1mol乙醇反应生成乙酸乙酯的分子数为0.1NA | |
| C. | 29g异丁烷中含有共价键数为6.5NA | |
| D. | 4.6g金属钠在空气中加热充分反应,转移电子数为0.2NA |
3.下列分离混合物常见的仪器:从左至右,用于分离操作正确的是( )
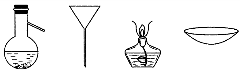

| A. | 蒸发、萃取、蒸馏、过滤 | B. | 蒸馏、过滤、蒸发、蒸发 | ||
| C. | 萃取、过滤、蒸馏、蒸发 | D. | 过滤、蒸发、萃取、蒸馏 |
20.下列说法错误的是(用NA代表阿伏加德罗常数的值)( )
| A. | 32g O2所含的原子数目为2NA | |
| B. | 0.5NA个氯气分子的物质的量是0.5mol | |
| C. | 在标准状况下,22.4 L CH4与18 g H2O所含有电子数均为10NA | |
| D. | 22.4 L的CO气体与1 mol N2所含的电子数相等 |
4.物质氧化性、还原性的强弱,不仅与物质的结构有关,还与浓度和反应温度有关,下列各组物质由于浓度不同而发生不同反应的是( )
| A. | Cu与HNO3 | B. | Cu与FeCl3 | C. | Zn与HCl | D. | FeCl3与NaOH |
1.在水溶液中下列电离方程式,正确的是( )
| A. | CH3COONH4?CH3COO-+NH4+ | B. | NaHCO3═Na++H++CO32- | ||
| C. | NaHSO4═Na++HSO4- | D. | CH3COOH?CH3COO-+H+ |
 .
.