题目内容
用以下三种途径来制取相等质量的硝酸铜:(1)铜跟浓硝酸反应;(2)铜跟稀硝酸反应;(3)铜先跟氧气反应生成氧化铜,氧化铜再跟硝酸反应.以下叙述正确的是( )
| A、三种途径所消耗的铜的物质的量相等 |
| B、三种途径所消耗的硝酸的物质的量相等 |
| C、所消耗的铜的物质的量是:途径(3)>途径(1)>途径(2) |
| D、所消耗的硝酸的物质的量是:途径(1)>途径(3)>途径(2) |
考点:硝酸的化学性质,铜金属及其重要化合物的主要性质
专题:元素及其化合物
分析:制取硝酸铜有关反应为:①Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O;
②3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O;
③2Cu+O2
2CuO,CuO+2HNO3(稀)=Cu(NO3)2+H2O
依据方程式判断生成相同质量的Cu(NO3)2,消耗原料的多少.
②3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O;
③2Cu+O2
| ||
依据方程式判断生成相同质量的Cu(NO3)2,消耗原料的多少.
解答:
解:制取硝酸铜有关反应为:①Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O;
②3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O;
③2Cu+O2
2CuO,CuO+2HNO3(稀)=Cu(NO3)2+H2O
从以上三组反应可以看出:生成相同质量的Cu(NO3)2,消耗相同质量的铜;
消耗硝酸的质量(或物质的量)不相同,途径①消耗HNO3最多,途径②次之,途径③消耗HNO3最少.
故答案为:A.
②3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O;
③2Cu+O2
| ||
从以上三组反应可以看出:生成相同质量的Cu(NO3)2,消耗相同质量的铜;
消耗硝酸的质量(或物质的量)不相同,途径①消耗HNO3最多,途径②次之,途径③消耗HNO3最少.
故答案为:A.
点评:本题考查硝酸铜的制备方案的评价,题目难度不大,注意要正确书写相关反应的化学方程式,题目可根据方程式进行判断.

练习册系列答案
相关题目
下列叙述错误的是( )
| A、化学是一门实用性很强的科学,支持了高技术的快速发展 |
| B、化学是一门探索那些肉眼看不见的粒子──原子、分子的特征和行为,引导人们认识整个物质世界的科学 |
| C、实验是学习化学、体验化学和探索化学过程的唯一途径 |
| D、运用像试管、烧杯、酒精灯等一类简单器具进行实验,从颜色的变化、沉淀的生成和溶解、气体的吸收和释放等现象,可推断体系的变化本质,研究物质构成的奥秘 |
下列电子式中,错误的是( )
| A、Na+ |
B、 |
C、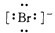 |
D、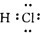 |
下列关于铵盐的叙述中正确的是( )
①所有铵盐中,氮元素化合价都是-3价;
②所有铵盐都溶于水;
③铵态氮肥不宜与草木灰混合使用;
④铵盐都是离子化合物;
⑤铵盐都能与碱反应,不能与酸反应.
①所有铵盐中,氮元素化合价都是-3价;
②所有铵盐都溶于水;
③铵态氮肥不宜与草木灰混合使用;
④铵盐都是离子化合物;
⑤铵盐都能与碱反应,不能与酸反应.
| A、①③④ | B、②③④ |
| C、①②③④ | D、①②③④⑤ |
下列既可以是原电池发生的电极反应式,又可以是电解池发生的电极反应式的是( )
①Cu-2e-=Cu2+ ②4OH--4e-=2H2O+O2↑ ③2H++2e-=H2↑
④Cu2++2e-=Cu ⑤2I--2e-=I2 ⑥2H2O+O2+4e-=4OH-.
①Cu-2e-=Cu2+ ②4OH--4e-=2H2O+O2↑ ③2H++2e-=H2↑
④Cu2++2e-=Cu ⑤2I--2e-=I2 ⑥2H2O+O2+4e-=4OH-.
| A、①②④⑥ | B、②③④⑤ |
| C、①③④ | D、②④⑥ |
能说明某烃分子里含有碳碳不饱和键的叙述中正确的是( )
| A、分子组成中含碳氢原子数比为1:2 |
| B、完成燃烧生产等物质的量的CO2和H2O |
| C、能与溴加成反应而使溴水褪色,还能使KMnO4酸性溶液褪色 |
| D、空气中燃烧能产生黑烟 |
 霉酚酸酯(MMF)是器官移植中抑制细胞增殖最常用的药物.下列说法正确的是( )
霉酚酸酯(MMF)是器官移植中抑制细胞增殖最常用的药物.下列说法正确的是( )| A、MMF能溶于水 |
| B、1 mol MMF能与含3 mol NaOH的水溶液完全反应 |
| C、1 mol MMF能与6 mol氢气发生加成反应 |
| D、MMF能发生取代反应和消去反应 |