题目内容
A~J分别表示中学化学中常见的物质,它们之间相互转化关系如图所示(部分反应物、生成物没有列出):
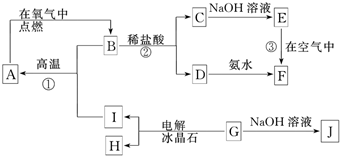
已知:A、B、C、D、E、F六种物质中均含有同一种元素;G为第ⅢA族元素形成的固态化合物,F为红褐色沉淀.
(1)写出物质的化学式:E F J
(2)写出反应的化学方程式:
① .
② .
③ .
(3)生成32g H需要转移 mol电子.

已知:A、B、C、D、E、F六种物质中均含有同一种元素;G为第ⅢA族元素形成的固态化合物,F为红褐色沉淀.
(1)写出物质的化学式:E
(2)写出反应的化学方程式:
①
②
③
(3)生成32g H需要转移
考点:无机物的推断
专题:推断题
分析:G为第ⅢA族元素形成的固态化合物,能与氢氧化钠反应反应,电解可以得到I、H,则G应为Al2O3,与NaOH反应生成J为NaAlO2,电解G生成O2和Al,F为红褐色沉淀,应为Fe(OH)3,则D为FeCl3,E为Fe(OH)2,C为FeCl2,所以B为Fe3O4,B与Al在高温下发生铝热反应生成A,则A为Fe,I为Al,故H为O2,据此解答.
解答:
解:G为第ⅢA族元素形成的固态化合物,能与氢氧化钠反应反应,电解可以得到I、H,则G应为Al2O3,与NaOH反应生成J为NaAlO2,电解G生成O2和Al,F为红褐色沉淀,应为Fe(OH)3,则D为FeCl3,E为Fe(OH)2,C为FeCl2,所以B为Fe3O4,B与Al在高温下发生铝热反应生成A,则A为Fe,I为Al,故H为O2,
(1)由上述分析可知,E为Fe(OH)2,F为Fe(OH)3,J为NaAlO2,故答案为:Fe(OH)2;Fe(OH)3;NaAlO2;
(2)反应①的化学方程式为:3Fe3O4+8Al
9Fe+4Al2O3 ;
反应②的化学方程式为:Fe3O4+8HCl=FeCl2+2FeCl3+4H2O;
反应③的化学方程式为:4Fe(OH)2+O2+2H2O=4Fe(OH)3,
故答案为:3Fe3O4+8Al
9Fe+4Al2O3;Fe3O4+8HCl=FeCl2+2FeCl3+4H2O;4Fe(OH)2+O2+2H2O=4Fe(OH)3;
(3)32g 氧气物质的量为1mol,故转移电子为1mol×4=4mol,故答案为:4.
(1)由上述分析可知,E为Fe(OH)2,F为Fe(OH)3,J为NaAlO2,故答案为:Fe(OH)2;Fe(OH)3;NaAlO2;
(2)反应①的化学方程式为:3Fe3O4+8Al
| ||
反应②的化学方程式为:Fe3O4+8HCl=FeCl2+2FeCl3+4H2O;
反应③的化学方程式为:4Fe(OH)2+O2+2H2O=4Fe(OH)3,
故答案为:3Fe3O4+8Al
| ||
(3)32g 氧气物质的量为1mol,故转移电子为1mol×4=4mol,故答案为:4.
点评:本题考查无机物的推断,涉及Fe、Al元素单质化合物性质,注意根据物质的性质和特殊反应进行推断,题目难度中等.

练习册系列答案
 寒假学与练系列答案
寒假学与练系列答案
相关题目
单质X能从盐溶液中转换出单质Y,由此可知( )
| A、当X、Y都是金属时,X不一定比Y活泼 |
| B、当X、Y都是非金属时,Y一定比X活泼 |
| C、当X是金属时,Y可能是金属也可能是非金属 |
| D、当X是非金属时,Y可能是金属也可能是非金属 |
下列离子方程式书写正确的是( )
| A、FeBr2溶液中通入少量的Cl2:2Br-+Cl2═2Cl-+Br2 |
| B、漂白粉溶液中通入过量的CO2:Ca2++2ClO-+2CO2+2H2O═CaCO3↓+2HClO+HCO3- |
| C、KHSO4溶液中加入Ba(OH)2溶液至中性:2H++SO42-+Ba2++2OH-═BaSO4↓+2H2O |
| D、氯化亚铁溶液中加入稀HNO3:3Fe2++4H++NO3-═3Fe3++2H2O+NO↑ |
已知在相同状况下,要使同一化学键断裂需要吸收的能量等于形成该化学键放出的能量.下列说法正确的是( )
| A、电解熔融的Al2O3可以制得金属铝和氧气,该反应是一个放出能量的反应 |
| B、水分解产生氢气和氧气时放出能量 |
| C、相同状况下,反应2SO2+O2=2SO3是一个放热反应,则反应2SO3=2SO2+O2是一个吸热反应 |
| D、氯化氢分解成氢气和氯气时需要吸收能量 |