题目内容
17.基准物质邻苯二甲酸氢钾(KHC8H4O4)可用于标定( )| A. | 酸 | B. | 碱 | C. | 还原剂 | D. | 氧化剂 |
分析 实验室很难配制准确浓度的NaOH溶液,需要用基准物质来标定,邻苯二甲酸氢钾溶液显酸性,邻苯二甲酸氢钾纯度高,组成稳定,且相对分子质量较大,容易精确称量和配制容易,常作标准溶液.
解答 解:邻苯二甲酸氢钾纯度高,组成稳定,且相对分子质量较大,容易精确称量和配制容易,常作标准溶液,所以能用邻苯二甲酸氢钾作为基准物质来标定NaOH溶液,故选B.
点评 本题考查了物质性质的分析,标定溶液浓度的方法和试剂选择,掌握基础是解题关键,题目较简单.

练习册系列答案
相关题目
7.表是元素周期表的一部分,针对表中的①~⑩中元素,用元素符号或化学式填空回答以下问题:
(1)在③~⑦元素中,原子半径最大的是Na,其离子的原子结构示意图为
(2)写出⑤和⑨最高价氧化物对应水化物间发生反应的离子方程式:Al(OH)3+OH-=AlO2-+2H2O.
(3)按要求写出下列两种物质的电子式:①的单质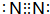 ;⑨的过氧化物
;⑨的过氧化物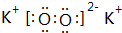 ;
;
(4)在⑦与⑩的单质中,化学性质较活泼的是Cl2,可用什么化学反应说明该事实(写出反应的化学方程式):Cl2+2NaBr=2NaCl+Br2.
(5)请用电子式表示④和⑩组成的化合物的形成过程 .
.
| 主族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 二 | ① | ② | ||||||
| 三 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ||
| 四 | ⑨ | ⑩ |

(2)写出⑤和⑨最高价氧化物对应水化物间发生反应的离子方程式:Al(OH)3+OH-=AlO2-+2H2O.
(3)按要求写出下列两种物质的电子式:①的单质
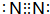 ;⑨的过氧化物
;⑨的过氧化物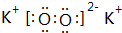 ;
;(4)在⑦与⑩的单质中,化学性质较活泼的是Cl2,可用什么化学反应说明该事实(写出反应的化学方程式):Cl2+2NaBr=2NaCl+Br2.
(5)请用电子式表示④和⑩组成的化合物的形成过程
 .
.
5.为测定空气中CO2含量,做下述实验:
(1)为配置标准溶液,请选取必需的一组仪器B;
①托盘天平 ②容量瓶 ③滴定管 ④量筒 ⑤烧杯 ⑥胶头滴管 ⑦玻璃棒
A、①②⑤⑥B、②④⑤⑥⑦C、①②⑥⑦D、②④⑤⑥
(2)滴定操作时,左手控制酸式滴定管活塞,眼睛注视液滴下滴速度和锥形瓶中溶液颜色的变化;
(3)取上述Ba(OH)2溶液10mL放入100mL容量瓶中,加水稀释至刻度,把稀释后的溶液放入密闭容器,并引入10L空气,振荡,过滤.需过滤的原因是除去BaCO3沉淀,使滤液只含Ba(OH)2,以保证实验成功;
(4)①本实验中,用0.1mol•L-1的标准盐酸滴定未知Ba(OH)2溶液时,由于操作不当,滴定结束后滴定管尖嘴处有一气泡,则实际用去盐酸大于19.60mL(填大于、小于、等于)
②若滴定Ba(OH)2溶液时使用的酸式滴定管未经处理,即换0.01mol•L-1盐酸溶液进行第二次滴定,导致算出空气中CO2值(填偏高、偏低或无影响)偏低.
(5)由实验数据算出空气中CO2的体积分数为0.025%.
| 配0.1mol/L的标准盐酸和0.01mol•L-1的标准盐酸 | → | 用0.1mol•L-1的标准盐酸滴定未知Ba(OH)2溶液10mL用去盐酸19.60mL | → | 用Ba(OH)2溶液吸收10L空气中的CO2(标准状况) | → | 过 滤 | → | 取滤液20mL,用0.01mol•L-1的盐酸滴定用去盐酸34.8mL |
①托盘天平 ②容量瓶 ③滴定管 ④量筒 ⑤烧杯 ⑥胶头滴管 ⑦玻璃棒
A、①②⑤⑥B、②④⑤⑥⑦C、①②⑥⑦D、②④⑤⑥
(2)滴定操作时,左手控制酸式滴定管活塞,眼睛注视液滴下滴速度和锥形瓶中溶液颜色的变化;
(3)取上述Ba(OH)2溶液10mL放入100mL容量瓶中,加水稀释至刻度,把稀释后的溶液放入密闭容器,并引入10L空气,振荡,过滤.需过滤的原因是除去BaCO3沉淀,使滤液只含Ba(OH)2,以保证实验成功;
(4)①本实验中,用0.1mol•L-1的标准盐酸滴定未知Ba(OH)2溶液时,由于操作不当,滴定结束后滴定管尖嘴处有一气泡,则实际用去盐酸大于19.60mL(填大于、小于、等于)
②若滴定Ba(OH)2溶液时使用的酸式滴定管未经处理,即换0.01mol•L-1盐酸溶液进行第二次滴定,导致算出空气中CO2值(填偏高、偏低或无影响)偏低.
(5)由实验数据算出空气中CO2的体积分数为0.025%.
12.设NA为阿伏加德罗常数的值,下列叙述正确的是( )

| A. | 常温常压下,16g 14CH4所含中子数目为8NA | |
| B. | 标准状况下,22.4 L CCl4所含分子数目为NA | |
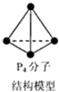
| C. | 6.2g白磷(分子式为P4,分子结构如图所示)所含P-P键数目为0.3NA | |
| D. | 1mol含8个碳原子的某烃分子,最多形成8NA个碳碳单键 |
2.NA表示阿伏伽德罗常数的值,下列说法正确的是( )
| A. | 6.4gCu在足量的硫蒸气中燃烧,转移的电子数为0.1NA | |
| B. | 标准状况下,11.2LSO2和SO3的混合物中硫原子数为0.5NA | |
| C. | 1L0.1mol•L-1的NH4Cl溶液中NH4+数目为0.1NA | |
| D. | 通常情况下,3.4gNH3中共用电子对数为0.8NA |
9.如表是Na、Mg、Si、S、Br五种元素的单质的沸点,其中b、e均是热和电的良导体.
(1)a呈深红棕色,a的元素在元素周期表中的位置为第四周期第VIIA族;
(2)写出d的元素原子的最外层电子排布式3s23p2;其元素原子核外中共有5种能量不同的电子;
(3)写出c的气态氢化物的水溶液与b的元素的最高价氧化物对应水化物反应的离子方程式H2S+2OH-=S 2-+H2O.
| 单质 | a | b | c | d | e |
| 沸点(℃) | 58.8 | 882.9 | 444.7 | 2 355 | 1 107 |
(2)写出d的元素原子的最外层电子排布式3s23p2;其元素原子核外中共有5种能量不同的电子;
(3)写出c的气态氢化物的水溶液与b的元素的最高价氧化物对应水化物反应的离子方程式H2S+2OH-=S 2-+H2O.
9.我国新修订的《环境保护法》已于2015年1月1日起施行.下列有关做法不正确的是( )
| A. | 用CO2合成聚碳酸酯等可降解塑料,以减少白色污染 | |
| B. | 减少生产、生活中产生的扬尘,以减少雾霾天气的形成 | |
| C. | 加强生活污水的脱氮、除磷处理,以遏制水体的富营养化 | |
| D. | 使用汽车尾气净化器.以减少二氧化碳的排放 |
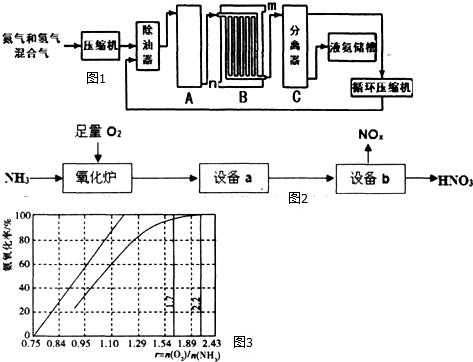
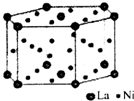 对物质性质的认识源于对其结构的了解.
对物质性质的认识源于对其结构的了解. .
.