题目内容
1.鉴别Na2CO3溶液和NaHCO3溶液的试剂是氯化钙或者氯化钡溶液,离子方程式为CO32-+Ca2+=CaCO3↓或CO32-+Ba2+=BaCO3↓.分析 二者阴离子不同,碳酸根离子与钙离子结合生成沉淀,而碳酸氢根离子不能,以此来解答.
解答 解:Na2CO3溶液和NaHCO3溶液不同的是阴离子,碳酸根离子能和钙离子或者钡离子反应生成沉淀,而碳酸氢跟和钙离子或者钡离子不反应,故选氯化钙或者氯化钡溶液,离子方程式为 CO32-+Ca2+=CaCO3↓或CO32-+Ba2+=BaCO3↓,
故答案为:氯化钙或者氯化钡溶液; CO32-+Ca2+=CaCO3↓或CO32-+Ba2+=BaCO3↓.
点评 本题考查物质的鉴别,为高频考点,把握物质的性质、发生的反应与现象为解答的关键,侧重分析与实验能力的考查,注意元素化合物知识与实验的结合,题目难度不大.

练习册系列答案
相关题目
11.下列关于某一化学反应的平衡常数的说法,正确的是( )
| A. | 与该反应的压强有关 | |
| B. | 与反应的温度有关,还与反应本身有关 | |
| C. | 与化学反应本身和温度有关,并且会受到起始浓度的影响 | |
| D. | 只与化学反应本身有关,与其他任何条件无关的一个不变的常数 |
12.下列各组物质中,互为同位素的是( )
| A. | D2O和H2O | B. | SO3和SO2 | C. | O3和O2 | D. | 235U和238U |
16.下列各组离子中,在碱性溶液中能大量共存,且溶液为无色透明的是( )
| A. | K+、MnO4-、Cl-、SO42- | B. | Na+、AlO2-、Cl-、SO42- | ||
| C. | SO42-、Fe3+、HCO3-、Ba2+ | D. | Mg2+、NO3-、NH4+、SO42- |
6.“84”消毒液在日常生活中使用广泛,该消毒液无色,有漂白作用.它的有效成分是( )
| A. | NaOH | B. | NaClO | C. | KMnO4 | D. | M2O2 |
13.表中对离子方程式的评价和理的是( )
| 选项 | 化学反应及对离子方程式 | 评价 |
| A | 金属钠加入滴有酚酞的水中:Na+H2O═Na++OH-+H2↑ | 正确 |
| B | 等体积等物质的量浓度的AlCl3、Ba(OH)2、HCl溶液混合:Al3+3H+6OH-═Al(OH)3↓+3H2O | 正确 |
| C | 向硅酸钠溶液中通入过量CO2:SiO32-+2H2O+2CO2═H2SiO3↓+2HC3-O | 错误,CO2过量溶液应该变澄清 |
| D | 向氯化钠铝溶液中加入足量氨水溶液:Al3++4NH3•H2O═AlO2+2H2O+4NH4+ | 正确 |
| A. | A | B. | B | C. | C | D. | D |
10.标况下,36gCO和CO2混合气体的体积为22.4L,关于该混合气体有下列的说法
①混合气体中两种气体的分子个数必为1:1
②混合气体两种气体的质量比为7:11
③混合气体中碳和氧的原子个数比为2:3
④混合气体的密度是氢气密度是18倍,
其中正确的是( )
①混合气体中两种气体的分子个数必为1:1
②混合气体两种气体的质量比为7:11
③混合气体中碳和氧的原子个数比为2:3
④混合气体的密度是氢气密度是18倍,
其中正确的是( )
| A. | ①②③ | B. | ①③④ | C. | ①②④ | D. | ①②③④ |
20.在下列反应中:A2(g)+B2(g)?2AB(g)△H<0当其达到平衡时,在如图所示的曲线中,符合勒夏特列原理的是( )
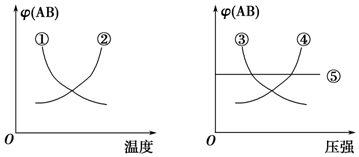

| A. | ①② | B. | ③④ | C. | ①④ | D. | ①⑤ |