题目内容
超细氧化镍(NiO)是一种功能材料,已被广泛用于电池电极、催化剂、半导体、玻璃染色剂等方面.工业上常以Ni(NO3)2?6H2O和尿素[CO(NH2)2]为原料制备.
(1)Ni2+的基态核外电子排布式为 .
(2)与NO3-离子互为等电子体的一种分子的分子式为 .
(3)尿素分子中碳原子的杂化方式为 ,1mol尿素分子中含有的σ键数为 .
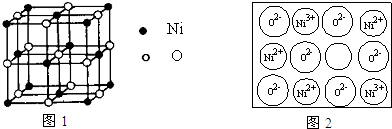
(4)NiO晶胞结构如图1所示,Ni的配位数为 .天然的和绝大部分人工制备的晶体都存在各种缺陷.某种NiO晶体中就存在如图2所示的缺陷:一个Ni2+空缺,另有两个Ni2+被两个Ni3+所取代.其结果晶体仍呈电中性,但化合物中Ni和O的比值却发生了变化.经测定某氧化镍样品中Ni3+与Ni2+的离子数之比为6:91.若该晶体的化学式为NixO,则x= .

(1)Ni2+的基态核外电子排布式为
(2)与NO3-离子互为等电子体的一种分子的分子式为
(3)尿素分子中碳原子的杂化方式为
(4)NiO晶胞结构如图1所示,Ni的配位数为
考点:晶胞的计算,配合物的成键情况
专题:化学键与晶体结构
分析:(1)Ni是28号元素,根据原子核外电子排布规律可知,Ni2+的基态核外电子排布式为1s22s22p63s23p63d8,据此答题;
(2)根据等电子体概念可知,原子数和价电子数都相等 的微粒互为等电子体,NO3-离子中有四个原子,价电子数为24,所以与NO3-离子互为等电子体的一种分子为BF3、SO3、COCl2等,据此答题;
(3)尿素分子的结构简式为: ,所以尿素分子中碳原子的杂化方式为sp2杂化,每个分子中含有7个σ键,据此答题;
,所以尿素分子中碳原子的杂化方式为sp2杂化,每个分子中含有7个σ键,据此答题;
(4)根据NiO晶胞结构可知,每个镍有6个氧,所以配位数为6,根据化合物化合价代数各为零,可以算出NixO中x的值;
(2)根据等电子体概念可知,原子数和价电子数都相等 的微粒互为等电子体,NO3-离子中有四个原子,价电子数为24,所以与NO3-离子互为等电子体的一种分子为BF3、SO3、COCl2等,据此答题;
(3)尿素分子的结构简式为:
 ,所以尿素分子中碳原子的杂化方式为sp2杂化,每个分子中含有7个σ键,据此答题;
,所以尿素分子中碳原子的杂化方式为sp2杂化,每个分子中含有7个σ键,据此答题;(4)根据NiO晶胞结构可知,每个镍有6个氧,所以配位数为6,根据化合物化合价代数各为零,可以算出NixO中x的值;
解答:
解:(1)Ni是28号元素,根据原子核外电子排布规律可知,Ni2+的基态核外电子排布式为1s22s22p63s23p63d8,故答案为:1s22s22p63s23p63d8;
(2)根据等电子体概念可知,原子数和价电子数都相等 的微粒互为等电子体,NO3-离子中有四个原子,价电子数为24,所以与NO3-离子互为等电子体的一种分子为BF3、SO3、COCl2等,故答案为:BF3、SO3、COCl2等;
(3)尿素分子的结构简式为: ,所以尿素分子中碳原子的杂化方式为sp2杂化,每个分子中含有7个σ键,所以1mol尿素中含有7moσ键,故答案为:sp2、7mol或7×6.02×1023个;
,所以尿素分子中碳原子的杂化方式为sp2杂化,每个分子中含有7个σ键,所以1mol尿素中含有7moσ键,故答案为:sp2、7mol或7×6.02×1023个;
(4)根据NiO晶胞结构可知,每个镍有6个氧,所以配位数为6;因为氧化镍样品中Ni3+与Ni2+的离子数之比为6:91,所以镍元素的平均价为
=
根据化合物化合价代数各为零,得
x=2,则x=0.97,故答案为:6、0.97;
(2)根据等电子体概念可知,原子数和价电子数都相等 的微粒互为等电子体,NO3-离子中有四个原子,价电子数为24,所以与NO3-离子互为等电子体的一种分子为BF3、SO3、COCl2等,故答案为:BF3、SO3、COCl2等;
(3)尿素分子的结构简式为:
 ,所以尿素分子中碳原子的杂化方式为sp2杂化,每个分子中含有7个σ键,所以1mol尿素中含有7moσ键,故答案为:sp2、7mol或7×6.02×1023个;
,所以尿素分子中碳原子的杂化方式为sp2杂化,每个分子中含有7个σ键,所以1mol尿素中含有7moσ键,故答案为:sp2、7mol或7×6.02×1023个;(4)根据NiO晶胞结构可知,每个镍有6个氧,所以配位数为6;因为氧化镍样品中Ni3+与Ni2+的离子数之比为6:91,所以镍元素的平均价为
| 6×3+91×2 |
| 6+91 |
| 200 |
| 97 |
| 200 |
| 97 |
点评:本题主要考查了核外电子的排布、等电子体、原子杂化、化学键、晶胞的计算等知识,中等难度,注重基础知识的考查.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
“下列食品添加剂与类别对应正确的是( )
| A、着色剂-苯甲酸钠 |
| B、调味剂-亚硝酸盐 |
| C、营养强化剂-粮食制品加赖氨酸 |
| D、防腐剂--胭脂红 |