题目内容
请探究第3周期元素性质是如何递变的?引起这种递变的本质原因是什么?
解析:
|
导思:研究元素性质的递变规律,必须先明确元素性质具体表现形式,然后从结构与性质的关系入手解决. 先要分析元素原子结构的规律性变化:同周期元素中,原子序数的递增对最外电子层的电子数、核电荷数的影响,核电荷数的增加对原子半径、核对外层电子的吸引力的影响. 这体现了结构决定性质和性质体现结构的辩证统一关系,也体现了量变引起质变的这一辩证规律. 探究:对于第3周期元素性质是如何递变的探究,可以探究金属钠、镁、铝与水和酸的反应以及它们的氢氧化物的碱性强弱,硅、磷、硫、氯与氢气化合的条件以及它们氢化物的稳定性,它们的最高价含氧酸的酸性强弱,还有氩的特殊稳定性,从而总结出递变规律. 随着元素原子序数的递增,同周期元素原子失电子的能力逐渐减弱,得电子的能力逐渐增强.引起这种变化的本质原因是元素原子结构的规律性变化:同周期元素中,随着原子序数的递增,最外电子层的电子数逐渐增多,同时,核电荷数也依次增加.在这个变化过程中,由于核电荷数的增加,使原子半径逐渐减小,使核对外层电子的吸引力逐渐增强,而结构的这一变化成了决定性质变化的主要影响因素.而到了稀有气体,由于原子的最外电子层已经达到了8个电子的稳定结构,所以,在一般情况下,它不容易得或失电子,而表现相对较稳定的性质. |

(10分)某同学做同周期元素性质递变规律实验时,设计了一套实验方案,并记录了有关实验现象(见下表,表中左右的“实验方案”与“实验现象”不一定是对应关系)。
| 实验方案 | 实验现象 |
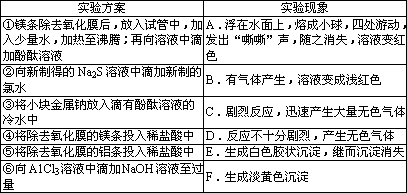
| ①镁条除去氧化膜后,放入试管中,加入少量水,加热至沸腾;再向溶液中滴加酚酞溶液 | A.浮在水面上,熔成小球,四处游动,发出“嘶嘶”声,随之消失,溶液变红色 |
| ②向新制得的Na2S溶液中滴加新制的氯水 | B.有气体产生,溶液变成浅红色 |
| ③将小块金属钠放入滴有酚酞溶液的冷水中 | C.剧烈反应,迅速产生大量无色气体 |
| ④将除去氧化膜的镁条投入稀盐酸中 | D.反应不十分剧烈,产生无色气体 |
| ⑤将除去氧化膜的铝条投入稀盐酸中 | E.生成白色胶状沉淀,继而沉淀消失 |
| ⑥向A1Cl3溶液中滴加NaOH溶液至过量 | F.生成淡黄色沉淀 |
请你帮助该同学整理并完成实验报告。
(1)实验目的:研究第3周期元素性质的递变规律。
(2)实验用品:
试剂:金属钠,镁条,铝条,稀盐酸,新制氯水,新制Na2S溶液,AlCl3溶液,NaOH
溶液,酚酞溶液等。
仪器:砂纸,试管,试管夹,① ,火柴,胶头滴管,烧杯,镊子,小刀,玻璃片,
② 等。
(3)实验内容:
| 实验方案 | ② | ④ | ⑥ |
| 实验现象(填A~F) |
|
|
|
①的化学方程式 ,
②的离子方程式 。
(4)实验结论: 。
(10分)某同学做同周期元素性质递变规律实验时,设计了一套实验方案,并记录了有关实验现象(见下表,表中左右的“实验方案”与“实验现象”不一定是对应关系)。
| 实验方案 | 实验现象 |
| ①镁条除去氧化膜后,放入试管中,加入少量水,加热至沸腾;再向溶液中滴加酚酞溶液 | A.浮在水面上,熔成小球,四处游动,发出“嘶嘶”声,随之消失,溶液变红色 |
| ②向新制得的Na2S溶液中滴加新制的氯水 | B.有气体产生,溶液变成浅红色 |
| ③将小块金属钠放入滴有酚酞溶液的冷水中 | C.剧烈反应,迅速产生大量无色气体 |
| ④将除去氧化膜的镁条投入稀盐酸中 | D.反应不十分剧烈,产生无色气体 |
| ⑤将除去氧化膜的铝条投入稀盐酸中 | E.生成白色胶状沉淀,继而沉淀消失 |
| ⑥向A1Cl3溶液中滴加NaOH溶液至过量 | F.生成淡黄色沉淀 |
(1)实验目的:研究第3周期元素性质的递变规律。
(2)实验用品:
试剂:金属钠,镁条,铝条,稀盐酸,新制氯水,新制Na2S溶液,AlCl3溶液,NaOH
溶液,酚酞溶液等。
仪器:砂纸,试管,试管夹,① ,火柴,胶头滴管,烧杯,镊子,小刀,玻璃片,
② 等。
(3)实验内容:
| 实验方案 | ② | ④ | ⑥ |
| 实验现象(填A~F) | | | |
①的化学方程式 ,
②的离子方程式 。
(4)实验结论: 。
(10分)某同学做同周期元素性质递变规律实验时,设计了一套实验方案,并记录了有关实验现象(见下表,表中左右的“实验方案”与“实验现象”不一定是对应关系)。
|
实验方案 |
实验现象 |
|
①镁条除去氧化膜后,放入试管中,加入少量水,加热至沸腾;再向溶液中滴加酚酞溶液 |
A.浮在水面上,熔成小球,四处游动,发出“嘶嘶”声,随之消失,溶液变红色 |
|
②向新制得的Na2S溶液中滴加新制的氯水 |
B.有气体产生,溶液变成浅红色 |
|
③将小块金属钠放入滴有酚酞溶液的冷水中 |
C.剧烈反应,迅速产生大量无色气体 |
|
④将除去氧化膜的镁条投入稀盐酸中 |
D.反应不十分剧烈,产生无色气体 |
|
⑤将除去氧化膜的铝条投入稀盐酸中 |
E.生成白色胶状沉淀,继而沉淀消失 |
|
⑥向A1Cl3溶液中滴加NaOH溶液至过量 |
F.生成淡黄色沉淀 |
请你帮助该同学整理并完成实验报告。
(1)实验目的:研究第3周期元素性质的递变规律。
(2)实验用品:
试剂:金属钠,镁条,铝条,稀盐酸,新制氯水,新制Na2S溶液,AlCl3溶液,NaOH
溶液,酚酞溶液等。
仪器:砂纸,试管,试管夹,① ,火柴,胶头滴管,烧杯,镊子,小刀,玻璃片,
② 等。
(3)实验内容:
|
实验方案 |
② |
④ |
⑥ |
|
实验现象(填A~F) |
|
|
|
①的化学方程式 ,
②的离子方程式 。
(4)实验结论: 。