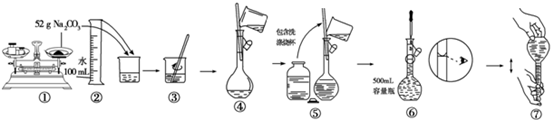
��Ŀ����
 Ϊ��������ЧӦ�����˼���CO2���ŷš�ֲ�����֡���Һ̬CO2ע����ȴ�ʩ�⣬����һ��˼·�ǽ�CO2ת����������ȼ���ʣ��繤ҵ����ʵ��CO2��H2��Ӧ���ɼ״���ת������֪����һ���¡������ܱ������г���l mol CO2��3mol H2��һ�������·�����Ӧ��CO2��g��+3H2��g��=CH3OH��g��+H2O��g����H=-49.0
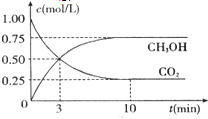
Ϊ��������ЧӦ�����˼���CO2���ŷš�ֲ�����֡���Һ̬CO2ע����ȴ�ʩ�⣬����һ��˼·�ǽ�CO2ת����������ȼ���ʣ��繤ҵ����ʵ��CO2��H2��Ӧ���ɼ״���ת������֪����һ���¡������ܱ������г���l mol CO2��3mol H2��һ�������·�����Ӧ��CO2��g��+3H2��g��=CH3OH��g��+H2O��g����H=-49.0kJ/mol�����CO2��CH3OH��g����Ũ����ʱ��仯��ͼ��ʾ����ش�
��1���ﵽƽ���ʱ����
��2�����жϸ÷�Ӧ�ﵽ��ѧƽ��״̬��������
a������ѹǿ���� b�����������c��CO2������
c��V��CH3OH��=V��H2O�� d��c��CH3OH��=c��H2O��
��3��Ϊ�����H2��ת���ʣ��ɲ�ȡ
��4����ƽ���H2��ת������
���㣺���ʵ�����Ũ����ʱ��ı仯����,��ѧƽ���Ӱ������,��ѧƽ��״̬���ж�
ר�⣺��ѧƽ��ר��
��������1���������ʵ�Ũ�Ȳ�����ʱ��ı仯���仯������Ӧ����ƽ��״̬������v=
���㷴Ӧ���ʣ�
��2������ƽ��״̬�������жϷ�Ӧ�Ƿ���ƽ��״̬��
��3�����ڿ��淴Ӧ����һ�ַ�Ӧ��Ũ��Ҫ���������һ�����ʵ�ת���ʣ��ݴ˴��⣻
��4����������ʽ����ת���ʺ�ƽ�ⳣ����
| ��c |
| t |
��2������ƽ��״̬�������жϷ�Ӧ�Ƿ���ƽ��״̬��
��3�����ڿ��淴Ӧ����һ�ַ�Ӧ��Ũ��Ҫ���������һ�����ʵ�ת���ʣ��ݴ˴��⣻
��4����������ʽ����ת���ʺ�ƽ�ⳣ����
���
�⣺��1���������ʵ�Ũ�Ȳ�����ʱ��ı仯���仯������Ӧ����ƽ��״̬����ͼ��֪���ڵ�10minʱ��Ũ�Ȳ��䣬����v=
��֪������̼��Ӧ����Ϊ
mol/��L?min��=0.075mol/��L?min�����ʴ�Ϊ��10��0.075mol/��L?min����
��2������ƽ��״̬�������жϷ�Ӧ�Ƿ���ƽ��״̬��
a�����ڸ÷�Ӧ�����������С�ķ�Ӧ�����Ե�����ѹǿ����ʱ���Ϳ�˵����Ӧ�Ѿ�����ƽ��״̬��
b�����������c��CO2������ʱ���������ʵ�Ũ��Ҳ���ٱ仯����Ӧ����ƽ��״̬��
c����V��CH3OH��=V��H2O���У����ܿ���������Ӧ���ʻ����淴Ӧ���ʣ������жϷ�Ӧ�Ƿ���ƽ��״̬��
d��c��CH3OH����c��H2O���Ĺ�ϵ����ʼ�������Ϊ�أ��뷴Ӧ�Ƿ���ƽ��״̬�أ��ʲ����жϷ�Ӧ�Ƿ���ƽ��״̬��
��ѡab��
��3�����ڿ��淴Ӧ����һ�ַ�Ӧ��Ũ��Ҫ���������һ�����ʵ�ת���ʣ��ʴ�Ϊ������
��4��������̼����ʼŨ��Ϊ1mol/L������������ʵ���Ϊ1mol�������������Ϊ1L��������������ʼŨ��Ϊ3mol/L��
��������ʽ���㣬��ͼ��֪������ݣ�
CO2��g��+3H2��g��=CH3OH��g��+H2O��g��
��ʼ��mol/L�� 1 3 0 0
ת����mol/L�� 0.75 2.25 0.75 0.75
ƽ�⣨mol/L�� 0.25 0.75 0.75 0.75
����H2��ת����Ϊ
��100%=75%
ƽ�ⳣ��K=
=
=5.3
�ʴ�Ϊ��75%��5.3��
| ��c |
| t |
| 1.0-0.25 |
| 10 |
��2������ƽ��״̬�������жϷ�Ӧ�Ƿ���ƽ��״̬��
a�����ڸ÷�Ӧ�����������С�ķ�Ӧ�����Ե�����ѹǿ����ʱ���Ϳ�˵����Ӧ�Ѿ�����ƽ��״̬��
b�����������c��CO2������ʱ���������ʵ�Ũ��Ҳ���ٱ仯����Ӧ����ƽ��״̬��
c����V��CH3OH��=V��H2O���У����ܿ���������Ӧ���ʻ����淴Ӧ���ʣ������жϷ�Ӧ�Ƿ���ƽ��״̬��
d��c��CH3OH����c��H2O���Ĺ�ϵ����ʼ�������Ϊ�أ��뷴Ӧ�Ƿ���ƽ��״̬�أ��ʲ����жϷ�Ӧ�Ƿ���ƽ��״̬��
��ѡab��
��3�����ڿ��淴Ӧ����һ�ַ�Ӧ��Ũ��Ҫ���������һ�����ʵ�ת���ʣ��ʴ�Ϊ������
��4��������̼����ʼŨ��Ϊ1mol/L������������ʵ���Ϊ1mol�������������Ϊ1L��������������ʼŨ��Ϊ3mol/L��
��������ʽ���㣬��ͼ��֪������ݣ�
CO2��g��+3H2��g��=CH3OH��g��+H2O��g��
��ʼ��mol/L�� 1 3 0 0
ת����mol/L�� 0.75 2.25 0.75 0.75
ƽ�⣨mol/L�� 0.25 0.75 0.75 0.75
����H2��ת����Ϊ
| 2.25 |
| 3 |
ƽ�ⳣ��K=
| 0.75��0.75 |
| 0.25��0.753 |
| 16 |
| 3 |
�ʴ�Ϊ��75%��5.3��
������������Ҫ�����˻�ѧ��Ӧ���ʵļ��㣬��ѧƽ���������ƽ�ⳣ���ļ����֪ʶ�㣬�е��Ѷȣ�����Ҫע�����֪ʶ�����ã�

��ϰ��ϵ�д�
�����Ŀ
�й��Ƶ�������ȷ���ǣ�������
| A��2.3g����97.7gˮ��Ӧ����Һ�����ʵ�������������4% |
| B���Ƹ�CuSO4��Һ��Ӧ���ɵ���ɫ��������ʱ���ְ��ߣ����������˽���ͭ |
| C����һС����Ͷ��ʢ���ͳ���ʯ��ˮ���Թ�����Һ����� |
| D�����ڿ����еĻ������������ڿ����е�ȼ�IJ��ﶼһ�� |
��ָ���������£����и�������һ���ܴ���������ǣ�������
| A����ɫ����Һ�У�Fe3+��K+��ClO-��Cl- |
| B��pH=12����Һ�У�NH4+��Na+��SO42-��Cl- |
| C��c��H+��=0.1 mol?L-1����Һ�У�NH4+��Fe2+��Cl-��NO3- |
| D�����д���Ba2+����Һ�У�K+��Na+��Cl-��OH- |