题目内容
12.在标准情况下,将aLA气体(摩尔质量为Mgmol-1)溶于1L水中,所得溶液密度为pg•cm-3则此溶液的质量为(1000+$\frac{Ma}{22.4}$)g.分析 根据n=$\frac{V}{{V}_{m}}$计算出aLA的物质的量,然后根据m=nM计算出溶质的质量;水的密度约为1g/mL,根据m=ρV计算出1L水的质量,从而可计算出溶液质量.
解答 解:标准状况下,aL该气体的物质的量为:$\frac{aL}{22.4L/mol}$=$\frac{a}{22.4}$mol,该溶液中含有A的质量为:Mg/mol×$\frac{a}{22.4}$mol=$\frac{Ma}{22.4}$g,
1L水的质量为:1g/mL×1000mL=1000g,
所以此溶液的质量为:$\frac{Ma}{22.4}$g+1000g=(1000+$\frac{Ma}{22.4}$)g,
故答案为:(1000+$\frac{Ma}{22.4}$).
点评 本题考查了物质的量的计算,题目难度不大,明确物质的量与摩尔质量、气体摩尔体积之间的关系为解答关键,注意题中没有告诉溶液体积,不能根据溶液密度计算溶液质量.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
2.将HCl和NaCl分别溶于水.下列说法正确的是( )
| A. | HCl的离子键被破坏 | B. | NaCl的共价键被破坏 | ||
| C. | HCl和NaCl的化学键均遭破坏 | D. | HCl和NaCl的化学键均未遭破坏 |
3.甲烷分子是以C原子为中心的正四面体结构,而不是正方形的平面结构,理由是( )
| A. | CH3Cl只代表一种物质 | B. | CH2Cl2只代表一种物质 | ||
| C. | CHCl3只代表一种物质 | D. | CCl4是非极性分子 |
17.下列反应的离子方程式书写正确的是( )
| A. | 向沸水中滴加饱和氯化铁溶液:Fe3++3H2O═Fe(OH)3↓+3H+ | |
| B. | 澄清石灰水与少量苏打溶液混合:Ca2++OH-+HCO3-═CaCO3↓+H2O | |
| C. | 碳酸钙溶于醋酸:CaCO3+2H+═Ca2++CO2↑+H2O | |
| D. | 氯化亚铁溶液中通入氯气:2Fe2++Cl2═2Fe3++2Cl- |
7.分子式为C8H8O2的含有苯环有机物,能与NaHCO3溶液反应生成气体,则符合上述条件的同分异构体(不考虑立体异构)有( )
| A. | 4种 | B. | 8种 | C. | 11种 | D. | 12种 |
4.自来水加工处理流程如图,下列有关说法不正确的是( ) 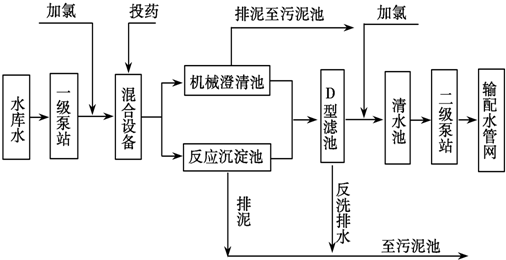

| A. | 若用FeSO4作混凝剂,最终铁将以Fe(OH)2形式进入反应沉淀池 | |
| B. | 投药时常加入适量的石灰,是为了除去水中Mg2+、HCO3-等 | |
| C. | 自来水生产中,前面加氯起消毒杀菌作用,后面加氯是保持水中有效氯的含量,防止自来水二次污染 | |
| D. | 用ClO2消毒自来水,消毒效率是等质量氯气的2.63倍 |
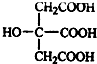 .
.
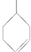 .
.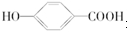 在一定条件下发生聚合反应生成高分子化合物,写出该反应的化学方程式(有机物写结构简式)
在一定条件下发生聚合反应生成高分子化合物,写出该反应的化学方程式(有机物写结构简式) .
.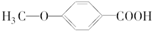 的同分异构体很多,其中符合下列条件的有3种.
的同分异构体很多,其中符合下列条件的有3种. .
.