题目内容
下列说法正确的是( )
| A、含有氧元素的化合物一定是氧化物 |
| B、在水溶液中能电离出H+的化合物一定是酸 |
| C、盐一定是有金属阳离子和酸根离子构成 |
| D、HCl不导电 |
考点:酸、碱、盐、氧化物的概念及其相互联系,电解质在水溶液中的电离
专题:电离平衡与溶液的pH专题
分析:A、依据氧化物概念分析,两种元素组成其中一种是氧元素的化合物为氧化物;
B、水溶液中电离出的阳离子全部是氢离子的化合物为酸;
C、盐也可以由非金属元素组成;
D、HCl不导电,溶于水电离出离子能导电;
B、水溶液中电离出的阳离子全部是氢离子的化合物为酸;
C、盐也可以由非金属元素组成;
D、HCl不导电,溶于水电离出离子能导电;
解答:
解:A、依据氧化物概念分析,两种元素组成其中一种是氧元素的化合物为氧化物,含有氧元素的化合物不一定是氧化物,如含氧酸,故A错误;
B、水溶液中电离出的阳离子全部是氢离子的化合物为酸,在水溶液中能电离出H+的化合物不一定是酸,如NaHSO4,故B错误;
C、盐也可以由非金属元素组成,如NH4Cl,故C错误;
D、HCl为共价化合物,熔融状态下不导电,溶于水电离出离子能导电,故D正确;
故选D.
B、水溶液中电离出的阳离子全部是氢离子的化合物为酸,在水溶液中能电离出H+的化合物不一定是酸,如NaHSO4,故B错误;
C、盐也可以由非金属元素组成,如NH4Cl,故C错误;
D、HCl为共价化合物,熔融状态下不导电,溶于水电离出离子能导电,故D正确;
故选D.
点评:本题考查了物质分类方法和物质性质,注意物质组成的理解应用,掌握基础是关键,题目较简单.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
下列各组物质中,属于同分异构体的是( )
| A、O2和O3 |
B、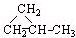 和CH3CH=CHCH3 和CH3CH=CHCH3 |
C、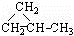 和CH2=CHCH3 和CH2=CHCH3 |
| D、CH3CH2OH和CH3OCH3 |
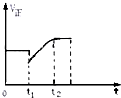 如图表示反应N2(g)+3H2(g)?2NH3(g)+Q的正反应速率随时间的变化情况,试根据如图曲线判断下列说法可能正确的是( )
如图表示反应N2(g)+3H2(g)?2NH3(g)+Q的正反应速率随时间的变化情况,试根据如图曲线判断下列说法可能正确的是( )| A、t1时只减小了压强 |
| B、t1时只降低了温度 |
| C、t1时减小了NH3的浓度,平衡向正反应方向移动 |
| D、t1时减小N2浓度,同时增加了NH3的浓度 |
学习方法中的类推法是由已学知识通过迁移构建新知识的方法.下列叙述正确的是( )
| A、Mg失火不能用CO2灭火,Na失火也不能用CO2灭火 |
| B、Al与S直接化合可以得到Al2S3,Fe与S直接化合也可以得到Fe2S3 |
| C、将SO2通入BaCl2溶液无白色沉淀生成,SO2通入Ba(NO3)2溶液也无白色沉淀生成 |
| D、工业上电解熔融MgCl2制取金属镁,也用电解熔融AlCl3的方法制取金属铝 |
下列叙述正确的是( )
| A、将稀氨水逐滴加入稀硫酸中,当溶液pH=7时,c(SO42-)>c(NH4+) | ||
| B、两种醋酸溶液的物质的量浓度分别为c1和c2,pH分别为a和a+1,则c1=10c2 | ||
| C、某种物质溶于水形成酸性溶液,该物质可能是强酸与强碱反应形成的盐 | ||
D、向0.1 mol/L的氨水中加入少量硫酸铵固体,则溶液中
|
分别用三份10ml0.1mol/L的AgNO3溶液可使体积比为3:2:1 的NaCl、MgCl2、AlCl3三种溶液反应中的氯离子恰好沉淀完全,三种溶液中Cl-的物质的量浓度之比为( )
| A、2:3:6 |
| B、1:2:3 |
| C、3:2:1 |
| D、1:1:1 |
下列有关常见有机化合物的说法正确的是( )
| A、将一小块金属钠投入无水乙醇中,钠块浮在液面上四处游动 |
| B、NaHCO3溶液可用于区分乙酸、乙醇和苯 |
| C、工业上,用乙醇和浓硫酸共热到170℃制取乙烯 |
| D、天然气的主要成分为甲烷,属于可再生能源 |
在100mL 0.1mol/L的MgCl2溶液中Cl-的物质的量浓度为( )
| A、0.01mol/L |
| B、0.02mol/L |
| C、0.1 mol/L |
| D、0.2 mol/L |