题目内容
13.为了说明影响化学反应快慢的因素,甲、乙、丙、丁四位学生分别设计了如下A-D四个实验,你认为结论不正确的是( )| A. | 将浓硝酸分别放在冷暗处和强光照射下,会发现强光照可以加快浓硝酸的分解 | |
| B. | 在相同条件下,等质量的大理石块和大理石粉与相同的盐酸反应,大理石粉反应快 | |
| C. | 将相同大小、形状的镁条和铝条与相同浓度的盐酸反应时,两者速率一样大 | |
| D. | 两支试管中分别加入相同质量的氯酸钾,其中一支试管中再加入少量二氧化锰,另一支试管不加;同时加热,产生氧气的快慢不同 |
分析 C.不同的金属,性质不同,为影响化学反应速率的主要因素;
A.浓硝酸在光照条件下易分解;
B.固体的表面积不同,化学反应速率不同;
D.催化剂能加快反应速率.
解答 解:A.浓硝酸在光照条件下易分解,光照时影响化学反应速率的条件之一,故A正确;
B.固体的表面积不同,化学反应速率不同,粉末状固体的表面积比块状固体表面积大,反应速率大,故B正确;
C.镁条和铝条的活泼性不同,与相同浓度盐酸反应,镁反应速率较大,故C错误;
D.催化剂能加快反应速率,在氯酸钾分解的试验中,二氧化锰起到催化剂的作用,故D正确;
故选C.
点评 本题考查外界条件对化学反应速率的影响,题目难度不大,注意B项,为易错点,物质的性质是影响化学反应速率的主要因素.

练习册系列答案
 计算高手系列答案
计算高手系列答案
相关题目
3.下列事实能判断金属元素甲的金属性一定比乙强的有( )
①甲单质能与乙盐的溶液反应并置换出乙
②甲、乙两元素原子的最外层电子数相同,且甲的原子半径小于乙
③甲、乙两短周期元素原子的电子层数相同,且甲的原子序数小于乙
④甲、乙两元素的最高价氧化物水化物的碱性甲大于乙.
①甲单质能与乙盐的溶液反应并置换出乙
②甲、乙两元素原子的最外层电子数相同,且甲的原子半径小于乙
③甲、乙两短周期元素原子的电子层数相同,且甲的原子序数小于乙
④甲、乙两元素的最高价氧化物水化物的碱性甲大于乙.
| A. | 全部可以 | B. | 仅②可以 | C. | 仅②③可以 | D. | ①③④可以 |
1.有机物的结构可用“键线式”表示,如:CH3CH=CHCH3可简写为 .有机物X的键线式为
.有机物X的键线式为 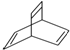 ,下列说法正确的是( )
,下列说法正确的是( )
 .有机物X的键线式为
.有机物X的键线式为  ,下列说法正确的是( )
,下列说法正确的是( )| A. | X的化学式为C8H10 | |
| B. | 有机物Y  与X互为同系物 与X互为同系物 | |
| C. | X因发生加成反应而使酸性高锰酸钾溶液褪色 | |
| D. | X与足量的H2在一定条件下反应可生成环状烃Z,Z的一氯代物有2种 |
8.若将海水淡化作饮用水使用,下列方法在原理上完全不可行的是( )
| A. | 加明矾使海水中的盐分沉淀而淡化 | |
| B. | 利用太阳能使海水蒸馏淡化 | |
| C. | 将海水缓慢凝固以获取淡化的饮用水 | |
| D. | 将海水通过离子交换树脂,以除去所含离子 |
18.某元素R在其氢氧化物和硝酸盐中的化合价均为+n,若上述两化合物的式量分别为M、N,则n为( )
| A. | $\frac{(N-M)}{45}$ | B. | $\frac{(M-N)}{45}$ | C. | $\frac{(M-N)}{90}$ | D. | $\frac{(N-M)}{90}$ |
5.在某酸性溶液中,能大量共存的离子组是( )
| A. | Na+、Al3+、SO42-、HCO3- | B. | Cu2+、Mg2+、SO42-、NO3- | ||
| C. | Na+、K+、ClO-、SO42- | D. | Fe3+、K+、SO42-、I- |
2.下列化学用语正确的是( )
| A. | 硫化氢分子的电子式: | B. | S2-的结构示意图: | ||
| C. | HClO的结构式:H-O-Cl | D. | NH4Cl的电子式: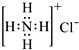 |
3.有机物分子中的原子(团)之间会相互影响,导致相同的原子(团)表现出不同的性质.下列现象不能说明上述观点的是( )
| A. | 苯酚与溴水可以直接反应,而苯与液溴反应则需要铁作催化剂 | |
| B. | 乙烯能与溴水发生加成反应,而乙烷不能与溴水发生加成反应 | |
| C. | 甲苯能使酸性KMnO4溶液褪色,而甲基环己烷不能使酸性KMnO4溶液褪色 | |
| D. | 苯酚可以与NaOH反应,而乙醇不能与NaOH反应 |