题目内容
7.四种多硼酸根离子的结构示意图如下,有关叙述正确的是( )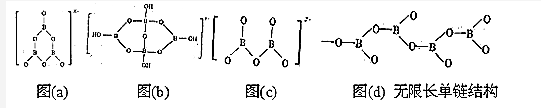
| A. | x=2 | B. | y=3 | ||
| C. | z=4 | D. | 图(d)的化学式为BO2 |
分析 A.B是+3价、O是-2价、H是+1价;
B.正负化合价代数和为0;
C.离子中正负化合价代数和为电荷数;
D.图(d)中最小重复结构单元为“BO2”.
解答 解:A.B是+3价、O是-2价、H是+1价,原子团“B3O6”带的负电荷数x=2×6-3×3=3,故A错误;
B.原子团“H4B4O9”带的负电荷数y=2×9-3×4-1×4=2,故B错误;
C.原子团“B2O5”带的负电荷数z=2×5-2×3=4,故C正确;
D.图(d)中最小重复结构单元为“BO2”,所带负电荷为2×2-1×3=1,化学式为(BO2)nn-或BO2-,故D错误.
故选C.
点评 本题考查化合价,明确分子中负化合价代数和为0,离子中正负化合价代数和为电荷数是解题的关键,题目难度不大.

练习册系列答案
相关题目
17.下列物质不属于有机物的是( )
| A. | 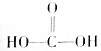 | B. | CO(NH2)2 | C. | CCl4 | D. | 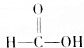 |
12.丙烯酸的结构简式为CH2=CH-COOH,下列关于丙烯酸的说法错误的是( )
| A. | 丙烯酸可以发生取代反应 | |
| B. | 丙烯酸可以使酸性高锰酸钾溶液褪色 | |
| C. | 丙烯酸与HBr发生加成反应只能得到唯一产物 | |
| D. | 丙烯酸钠溶液中Na+浓度大于丙烯酸根离子浓度 |
7.某恒温密闭容器中,可逆反应A(s)?B+C(g)△H=+Q kJ•mol-1(Q>0)达到平衡.缩小容器体积,重新达到平衡时,C(g)的浓度与缩小体积前的平衡浓度相等.以下分析正确的是( )
| A. | 产物B的状态只能为固态或液态 | |
| B. | 平衡时,单位时间内n(A)消耗﹕n(C)消耗=1﹕1 | |
| C. | 若开始时向容器中加入1molB和1molC,达到平衡时放出热量等于Q kJ | |
| D. | 保持体积不变,向平衡体系中加入A,平衡向正反应方向移动 |
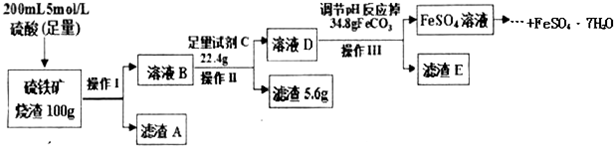
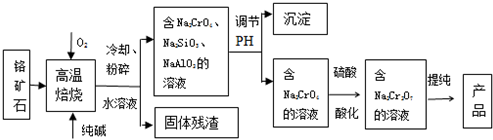
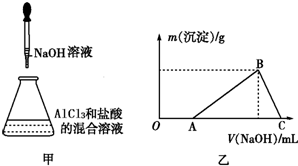 某同学称取一定质量的AlCl3固体配成溶液,在该溶液中加入一定量的稀盐酸,然后向此混合溶液中逐滴加入NaOH溶液如图甲所示.滴加过程中产生沉淀的质量与加入NaOH溶液的体积的关系如图乙所示.
某同学称取一定质量的AlCl3固体配成溶液,在该溶液中加入一定量的稀盐酸,然后向此混合溶液中逐滴加入NaOH溶液如图甲所示.滴加过程中产生沉淀的质量与加入NaOH溶液的体积的关系如图乙所示.